5Opción A
2 puntosContesta solo uno de los dos apartados: 5A o 5B.
El amoníaco y las disoluciones acuosas de este gas desprenden un olor irritante y muy característico que se nota, por ejemplo, en los productos empleados para limpiar cristales. La industria química fabrica cada día miles de toneladas de amoníaco mediante la siguiente reacción química entre el dinitrógeno y el dihidrógeno:
Hemos realizado un experimento en el laboratorio en el cual tenemos inicialmente los tres compuestos en equilibrio químico dentro de un recipiente. En un tiempo determinado, hemos adicionado dihidrógeno al recipiente y, mediante un conjunto de sensores conectados al sistema, hemos medido la concentración de los tres compuestos en función del tiempo, a temperatura constante, y hemos obtenido el gráfico siguiente:
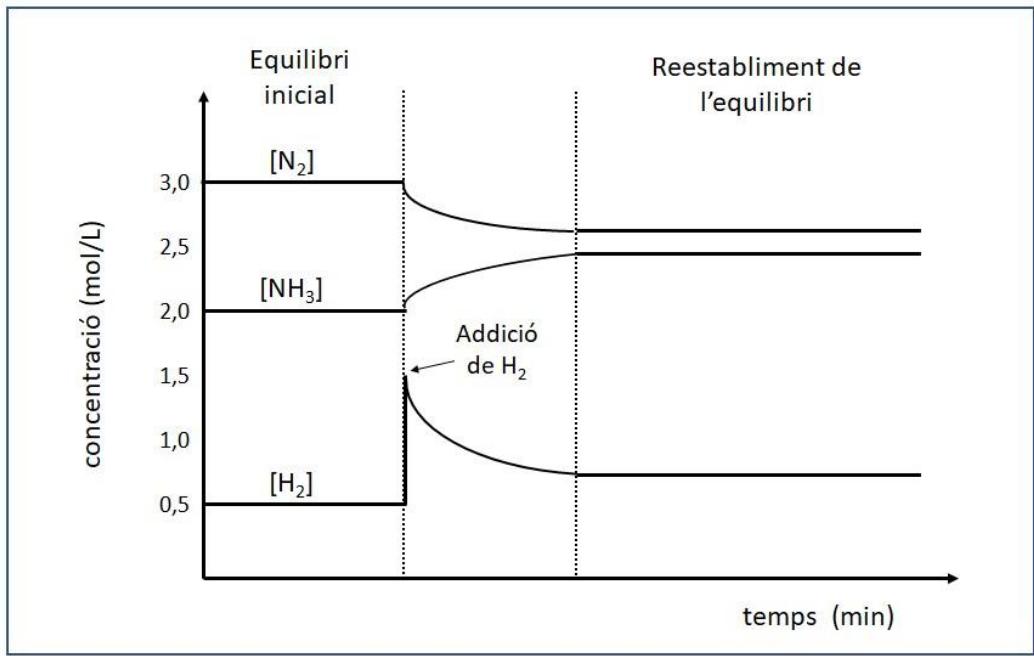
Calcula la constante de equilibrio en concentraciones () de la reacción de obtención de amoníaco, a la temperatura a la cual se ha efectuado el estudio.
Explica de forma razonada la modificación de la concentración de cada uno de los tres compuestos después de la adición de dihidrógeno dentro del recipiente.
¿Es cierto que un aumento de la temperatura del sistema favorecerá la obtención de amoníaco? Justifica la respuesta.
