A partir de la estructura química de la fenilalanina (figura 2), determina su masa molecular.
QuímicaBalearesPAU 2025Ordinaria
Química · Baleares 2025
9 ejercicios90 min de duración
Ejercicio 1
1
2 puntosEl premio Nobel de Química del año 2024 fue otorgado conjuntamente a los investigadores David Baker, Demis Hassabis y John M. Jumper por el desarrollo de un modelo basado en inteligencia artificial que permite predecir la estructura compleja de las proteínas (figura 1). Uno de los aminoácidos esenciales presentes en la estructura de las proteínas de los seres vivos es la fenilalanina (figura 2).

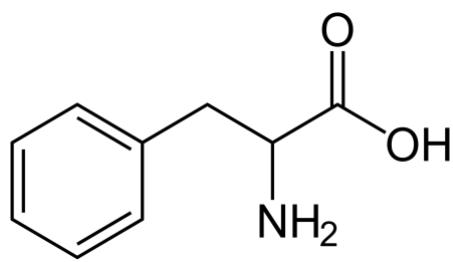
La fenilalanina puede actuar como un ácido monoprótico del tipo con una . En el caso de tener una disolución acuosa de fenilalanina, ¿cuál sería su pH?
Formula los compuestos siguientes: (i) tolueno o metilbenceno; (ii) ciclohexano.
Indica el significado del pictograma siguiente, que aparece en la ficha de seguridad del tolueno.

Ejercicio 2 · Opción A
2Opción A
2 puntosContesta solo uno de los dos apartados: 2A o 2B.
Los halógenos son los elementos del grupo 17 de la tabla periódica y se caracterizan porque tienen siete electrones en la capa de valencia.
| 9 F Flúor 18,998 |
| 17 Cl Cloro 35,453 |
| 35 Br Bromo 79,904 |
El tetracloruro de carbono () es un disolvente orgánico apolar. Justifica la geometría y el carácter apolar de este compuesto a partir del modelo de repulsión de los pares de electrones de la capa de valencia (TRPEV).
Indica, de manera razonada, cuál de los dos enlaces, o , presentará una mayor longitud.
El triclorometano () es líquido a , mientras que el tribromometano () es un sólido a esta misma temperatura. ¿Cómo justificas este hecho?
Ejercicio 2 · Opción B
2Opción B
2 puntosContesta solo uno de los dos apartados: 2A o 2B.
Los elementos , , y pertenecen al tercer periodo de la tabla periódica y tienen, respectivamente, 1, 2, 6 y 7 electrones en la capa de valencia.
¿Cuál de los cuatro elementos anteriores presenta la energía de ionización más elevada? Justifica la respuesta.
Razona cuáles serán los iones monoatómicos más estables de los elementos y .
Formula el compuesto que previsiblemente formará el con el e indica el tipo de enlace existente en este compuesto.
Razona el tipo de enlace que se establecerá entre el y el cuando estos dos compuestos reaccionen entre sí para formar dicloruro de azufre (). ¿Se trata de un compuesto polar o apolar? Justifica la respuesta.
Ejercicio 3 · Opción A
3Opción A
2 puntosContesta solo uno de los dos apartados: 3A o 3B.
El descubrimiento del ácido acético o ácido etanoico () como una sustancia química tuvo lugar en el siglo XVIII. En 1782, el químico sueco Karl Wilhelm Scheele fue el primero en aislar y describir el ácido acético en su forma líquida.
En un laboratorio, se valoran de una disolución de ácido acético con una disolución de hidróxido de potasio ():
Calcula el volumen de la disolución de que se necesitará para alcanzar el punto de equivalencia.
Razona si el valor del pH, en el punto de equivalencia, será mayor o menor que 7.
Explica, indicando el material necesario y el procedimiento seguido, cómo prepararías en el laboratorio de una disolución de ácido acético a partir de la disolución del enunciado.
Ejercicio 3 · Opción B
3Opción B
2 puntosContesta solo uno de los dos apartados: 3A o 3B.
El benceno () es un hidrocarburo peligroso, ya que emite vapores tóxicos, los cuales pueden producir cáncer. Este compuesto se encuentra presente en el humo del tabaco.
La reacción de combustión del benceno es la siguiente:
| Sustancia | H2O (l) | CO2 (g) | C6H6 (l) | C6H6 (g) |
| ΔH°f (kJ mol-1) | -286 | -394 | +49 | +83 |
Calcula la entalpía estándar a de la reacción de combustión del benceno a partir de los datos de la tabla 1. Indica si el proceso es endotérmico o exotérmico.
El benceno es un hidrocarburo que se puede vaporizar en condiciones estándar a . Calcula la energía necesaria para vaporizar de benceno líquido a partir de los datos de la tabla 1.
Ejercicio 4 · Opción A
4Opción A
2 puntosContesta solo uno de los dos apartados: 4A o 4B.
Una pila electroquímica es un dispositivo experimental con el cual se puede generar electricidad mediante una reacción química de oxidación-reducción.
Se construye una pila con la notación siguiente:
Haz un dibujo del montaje experimental de la pila.
Escribe las reacciones que tienen lugar en el ánodo y en el cátodo de la pila.
Indica, de forma razonada, si este proceso redox será espontáneo.
¿Cuáles son las funciones del puente salino?
Ejercicio 4 · Opción B
4Opción B
2 puntosContesta solo uno de los dos apartados: 4A o 4B.
Indica si las afirmaciones siguientes son verdaderas o falsas. Justifica, para cada uno de los casos, tu respuesta.
La velocidad de una reacción química se puede expresar en .
La energía de activación de una reacción química disminuye cuando aumenta la temperatura.
Cuando añadimos un catalizador a una reacción química el valor de la entalpía de reacción () disminuye.
La velocidad de una reacción química depende del estado de agregación en que se encuentran los reactivos.
Ejercicio 5 · Opción A
5Opción A
2 puntosContesta solo uno de los dos apartados: 5A o 5B.
El amoníaco y las disoluciones acuosas de este gas desprenden un olor irritante y muy característico que se nota, por ejemplo, en los productos empleados para limpiar cristales. La industria química fabrica cada día miles de toneladas de amoníaco mediante la siguiente reacción química entre el dinitrógeno y el dihidrógeno:
Hemos realizado un experimento en el laboratorio en el cual tenemos inicialmente los tres compuestos en equilibrio químico dentro de un recipiente. En un tiempo determinado, hemos adicionado dihidrógeno al recipiente y, mediante un conjunto de sensores conectados al sistema, hemos medido la concentración de los tres compuestos en función del tiempo, a temperatura constante, y hemos obtenido el gráfico siguiente:
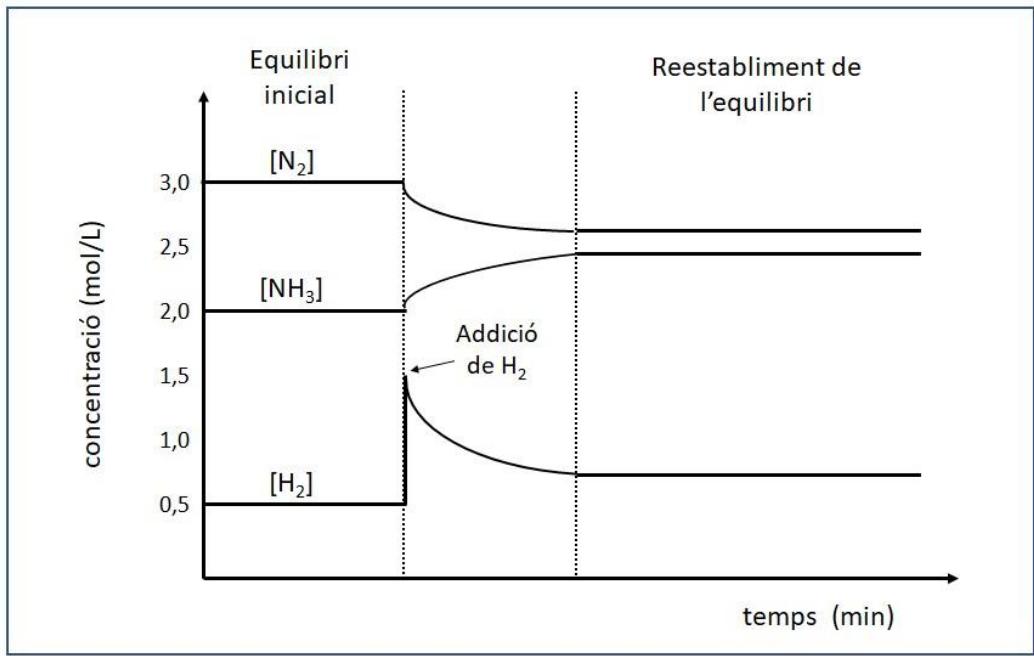
Calcula la constante de equilibrio en concentraciones () de la reacción de obtención de amoníaco, a la temperatura a la cual se ha efectuado el estudio.
Explica de forma razonada la modificación de la concentración de cada uno de los tres compuestos después de la adición de dihidrógeno dentro del recipiente.
¿Es cierto que un aumento de la temperatura del sistema favorecerá la obtención de amoníaco? Justifica la respuesta.
Ejercicio 5 · Opción B
5Opción B
2 puntosContesta solo uno de los dos apartados: 5A o 5B.
Los óxidos de nitrógeno forman parte de la polución de las grandes ciudades a causa de la reacción que se produce en los motores de combustión. Estos óxidos, principalmente el dióxido de nitrógeno () y el tetraóxido de dinitrógeno (), son responsables del llamado smog urbano. De entre estos compuestos, el es el más irritante para las vías respiratorias de las personas.
A , el se descompone y forma según la reacción química siguiente:
En un recipiente de de capacidad se dispone de una cierta cantidad de . El sistema se calienta hasta una temperatura de . Una vez alcanzado el equilibrio químico, la presión total dentro del recipiente es de y la presión parcial del es de .
Calcula el valor de a .
Determina el número de moles del compuesto en equilibrio.
Justifica, considerando cómo afecta la temperatura al equilibrio de descomposición del , si es previsible que un smog formado únicamente por una mezcla de los gases y sea más irritante en verano que en invierno.
