3Opción A
2 puntosEl diamante y el grafito son dos sustancias sólidas formadas solo por átomos de carbono que reciben la denominación de variedades alotrópicas del carbono. La diferencia fundamental en sus propiedades se debe a la disposición espacial de los átomos de carbono.
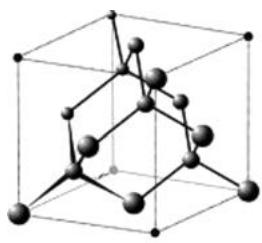

Calculad la variación de energía libre estándar, , de la transformación química siguiente a , y justificad si es espontánea:
La entalpía estándar de combustión del carbono grafito, a , es . Escribid la reacción de combustión del carbono grafito y calculad la masa mínima que debemos quemar de este compuesto para que el calor liberado se pueda utilizar para calentar de agua contenidos en una olla abierta, a y a presión atmosférica, hasta la temperatura de ebullición. Considerad negligible el calor absorbido por el recipiente.
