7Serie 4
2 puntosSerie 4
Elija UNA cuestión de entre la 6 y la 7.
La electrólisis del agua se puede efectuar con un voltámetro de Hofmann, como se muestra en la figura:
En uno de los electrodos se obtiene oxígeno según la semirreacción siguiente:
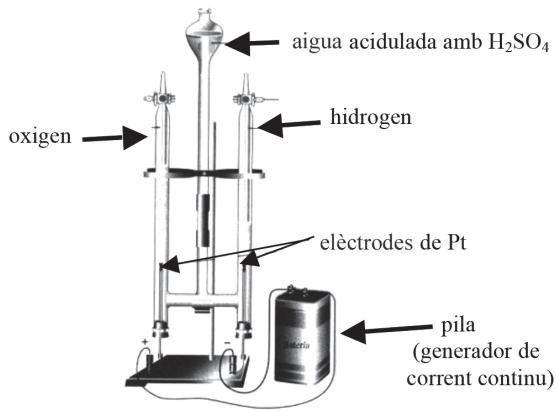
Escriba la semirreacción que tiene lugar en el otro electrodo e indique la polaridad de cada electrodo. ¿Qué gas se produce en el ánodo y cuál en el cátodo? ¿En todos los procesos electrolíticos es necesario suministrar energía mediante una pila? Justifique las respuestas.
El número de Avogadro (), que indica el número de partículas que contiene un mol de partículas, se puede obtener de manera experimental mediante una electrólisis. En el laboratorio hemos llevado a cabo una electrólisis de agua; hemos suministrado a la celda electrolítica una corriente eléctrica de durante y hemos obtenido de oxígeno, medidos a y . Calcule el número de Avogadro.
