Determine el orden de reacción respecto a cada reactivo y la constante de velocidad de la reacción a . Escriba la ecuación de velocidad de la reacción a .
QuímicaCataluñaPAU 2019Ordinaria
Química · Cataluña 2019
14 ejercicios90 min de duración
Ejercicio 1 · Serie 1
1Serie 1
2 puntosSerie 1
El dióxido de nitrógeno y el monóxido de carbono reaccionan en fase gaseosa según la ecuación siguiente:
Para poder predecir el mecanismo de esta reacción química a una determinada temperatura, es necesario conocer previamente cuál es su ecuación de velocidad. En un estudio cinético de esta reacción efectuado en un reactor de , y manteniendo la temperatura fija a , hemos obtenido los datos experimentales siguientes:
| Experimento | Masa inicial de (g) | Masa inicial de (g) | Velocidad inicial () |
| 1 | 23,00 | 56,00 | |
| 2 | 69,00 | 56,00 | |
| 3 | 69,00 | 28,00 | |
| 4 | 69,00 | 14,00 |
¿Qué sucede con la velocidad de la reacción si aumentamos la temperatura y mantenemos constante el volumen? ¿Y si aumentamos el volumen y mantenemos constante la temperatura? Justifique las respuestas utilizando el modelo cinético de colisiones.
Ejercicio 1 · Serie 4
1Serie 4
2 puntosSerie 4
El uso de la nanotecnología en el ámbito de la medicina es actualmente un campo de investigación puntero. Se han construido nanomotores propulsados por oxígeno gaseoso obtenido a partir de la descomposición del peróxido de hidrógeno, según la ecuación química siguiente:
Indique si la reacción de descomposición del peróxido de hidrógeno es espontánea en condiciones estándar y a , y si la espontaneidad de la reacción depende de la temperatura. Justifique las respuestas.
Nota: Suponga que la entalpía y la entropía estándar no varían en función de la temperatura.
En uno de los experimentos se demostró que las nanopartículas adquieren más velocidad cuando son iluminadas con radiaciones electromagnéticas con longitudes de onda de y . ¿Cuál de las dos radiaciones es más energética? ¿Con qué tipo de radiación electromagnética estamos iluminando las nanopartículas? Razone las respuestas.
| Frecuencia (Hz) | |||||
| Radiación | Rayos | Rayos X | Radiación ultravioleta y visible | Radiación infrarroja | Microondas |
Ejercicio 2 · Serie 1
2Serie 1
2 puntosSerie 1
Hemos montado una pila en el laboratorio empleando una solución concentrada de nitrato de potasio como puente salino. La reacción redox global que tiene lugar es la siguiente:
Escriba las semirreacciones que se producen en cada electrodo, y especifique cuál es el ánodo y cuál el cátodo. Escriba también la notación de la pila.
Razone hacia dónde se mueven los iones del puente salino. Calcule la fuerza electromotriz (FEM) de la pila en condiciones estándar y a .
Ejercicio 2 · Serie 4
2Serie 4
2 puntosSerie 4
Unos estudiantes que hacen un experimento en el laboratorio han querido comprobar si el magnesio y el cobre pueden generar hidrógeno cuando cada uno de estos metales reacciona separadamente con una solución acuosa de ácido clorhídrico diluido. Los experimentos que han llevado a cabo demuestran que solo uno de los dos metales reacciona con el ácido.
Justifique los resultados experimentales, identifique el metal que reacciona con el ácido y escriba la reacción.
En otro experimento construyen, en condiciones estándar y a , una pila formada por los pares redox y . Escriba las reacciones que tienen lugar en el ánodo y en el cátodo, y la reacción iónica global de la pila. Calcule también la fuerza electromotriz (FEM) de esta pila.
Ejercicio 3 · Serie 1
3Serie 1
2 puntosSerie 1
En octubre de 2018 entró en vigor la aplicación de una nueva normativa de etiquetado de los combustibles. La gasolina, que contiene isooctano (), ahora se etiqueta con un círculo donde figura el símbolo E5, E10 o E85, según contenga un , un o el de etanol, respectivamente.
Cuando se quema de isooctano a presión constante, en condiciones estándar y a , se obtienen de energía en forma de calor. Escriba la reacción de combustión del etanol líquido y justifique, a partir de los cálculos necesarios, si al quemar de etanol en las mismas condiciones se obtiene más o menos energía en forma de calor.
| Sustancia | etanol(l) | ||
| () | -264 | -278 | -393 |
Explique de qué peligros nos alertan estos cuatro pictogramas que encontramos en la etiqueta de un bidón de gasolina E5:




Ejercicio 3 · Serie 4
3Serie 4
2 puntosSerie 4
La codeína () se obtiene a partir del opio y se utiliza para combatir la tos y el dolor; también se usa, combinada con otros analgésicos, para incrementar el efecto de estos fármacos. Es un compuesto con propiedades básicas y en solución acuosa reacciona de la manera siguiente:
Cuando disolvemos un fármaco con un poco de agua obtenemos una solución acuosa de codeína . Calcule el pH de esta solución a .
Valoramos un jarabe incoloro que contiene codeína con una solución de ácido clorhídrico. Indique, razonadamente, si el pH en el punto de equivalencia es ácido, neutro o básico. Diga cuáles de los indicadores siguientes podríamos utilizar para detectar el punto final de esta valoración y justifique las respuestas.
| Indicadores ácido-base | |
| Nombre | Intervalo de viraje (pH) |
| rojo de metilo | 4,8-6,0 |
| fenolftaleína | 8,0-9,6 |
| amarillo de alizarina | 10,1-12,0 |
Ejercicio 4 · Serie 1
4Serie 1
2 puntosSerie 1
Elija UNA cuestión de entre la 4 y la 5.
El salfumán (solución acuosa de ácido clorhídrico, ) y el amoníaco son algunas de las sustancias que se utilizan habitualmente en la limpieza del hogar: la primera porque actúa como desinfectante y bactericida y la segunda porque elimina bien las grasas.
Calcule el pH, a , de una solución acuosa de amoníaco .
Escriba la reacción que se produce al mezclar una solución acuosa de amoníaco con salfumán. Explique el procedimiento experimental que seguiría en el laboratorio para determinar la entalpía de esta reacción e indique el material que utilizaría.
Ejercicio 4 · Serie 4
4Serie 4
2 puntosSerie 4
Elija UNA cuestión de entre la 4 y la 5.
El dióxido de azufre se origina por combustión de carbones o petróleos que contienen azufre como impureza. Este óxido se transforma en trióxido de azufre, y cuando se mezcla con vapor de agua produce ácido sulfúrico, uno de los componentes principales de la lluvia ácida. Observe la reacción siguiente:
A una temperatura determinada, esta reacción se puede dar directamente en una sola etapa (mecanismo A) o bien, de manera mucho más rápida, en presencia de monóxido de nitrógeno (mecanismo B).
Dibuje, de manera aproximada, un gráfico de la energía respecto a la coordenada de reacción para el mecanismo A, y otro gráfico para el mecanismo B. Indique en los gráficos las energías de activación, los estados de transición (complejo activado) y la variación de entalpía de la reacción global.
Los estudios cinéticos demuestran que la oxidación del dióxido de azufre a trióxido de azufre es una reacción de orden 1 respecto al oxígeno, y de orden 2 respecto al dióxido de azufre. Escriba la ecuación de velocidad de la reacción y deduzca las unidades de la constante de velocidad. Explique qué función realiza el monóxido de nitrógeno en el mecanismo B.
Ejercicio 5 · Serie 1
5Serie 1
2 puntosSerie 1
Elija UNA cuestión de entre la 4 y la 5.
El benceno, , es un hidrocarburo que se utiliza industrialmente como intermediario para fabricar otras sustancias químicas. Se ha comprobado experimentalmente que su punto de fusión es de a , su punto triple es de a y su punto crítico es de a .
Dibuje el diagrama de fases aproximado del benceno e indique en él los puntos de los cuales tenemos datos experimentales.
Justifique si el proceso de vaporización del benceno en condiciones estándar y a es espontáneo. Suponga que las variaciones de entalpía y entropía estándar del proceso de vaporización del benceno se mantienen constantes en el intervalo de temperatura entre y .
Ejercicio 5 · Serie 4
5Serie 4
2 puntosSerie 4
Elija UNA cuestión de entre la 4 y la 5.
El oxígeno () es un gas que se utiliza en diferentes actividades industriales y sanitarias, y almacenarlo y transportarlo requiere unas medidas de seguridad importantes. En la tabla siguiente se muestran unos cuantos datos del oxígeno:
| Punto de fusión | Punto de ebullición | Punto triple | Punto crítico |
| 55 K | 90 K | 54 K | 154 K |
| 1 atm | 1 atm | atm | 49,8 atm |
Defina el término punto triple de una sustancia. Haga un dibujo aproximado del diagrama de fases del oxígeno, y marque en él los cuatro puntos que figuran en la tabla.
La ficha de seguridad del oxígeno contiene los símbolos siguientes:
¿Qué quieren decir estos símbolos y de qué peligros nos advierten?



Ejercicio 6 · Serie 1
6Serie 1
2 puntosSerie 1
Elija UNA cuestión de entre la 6 y la 7.
El magnesio se utiliza para proteger las tuberías subterráneas de la corrosión. Este procedimiento químico, llamado protección catódica, se lleva a cabo soldando trozos de magnesio a las tuberías de hierro.
¿En qué consiste el proceso de corrosión de un metal? Justifique por qué el magnesio protege las tuberías de hierro subterráneas.
El magnesio metálico se puede obtener mediante la electrólisis de cloruro de magnesio fundido. Justifique qué sustancia gaseosa se produce en el ánodo en este proceso electrolítico. ¿Qué volumen de este gas obtendremos, medido a y , si se hace pasar una corriente de durante a través del cloruro de magnesio fundido?
Ejercicio 6 · Serie 4
6Serie 4
2 puntosSerie 4
Elija UNA cuestión de entre la 6 y la 7.
El propano y el butano son combustibles que se utilizan en los hogares y en la industria. Se pueden licuar fácilmente a presión, y esto facilita que se puedan transportar y vender envasados en bombonas.
Escriba las reacciones de combustión del propano y del butano. Queremos obtener de energía en forma de calor mediante la combustión de butano o propano a una presión constante de . ¿Cuál de los dos procesos de combustión genera menos cantidad de dióxido de carbono?
Calcule la masa de agua a que se puede calentar hasta si quemamos de butano a una presión constante de .
Ejercicio 7 · Serie 1
7Serie 1
2 puntosSerie 1
Elija UNA cuestión de entre la 6 y la 7.
La acetona, también conocida como propanona, es una sustancia de bajo punto de ebullición () y miscible en agua. Se puede obtener industrialmente mediante la reacción de deshidrogenación del propan-2-ol, también llamado 2-propanol, según la reacción química siguiente en fase gaseosa:
Para fabricar la máxima cantidad de acetona, ¿conviene trabajar a temperaturas altas o bajas? ¿A presiones altas o bajas? Justifique las respuestas.
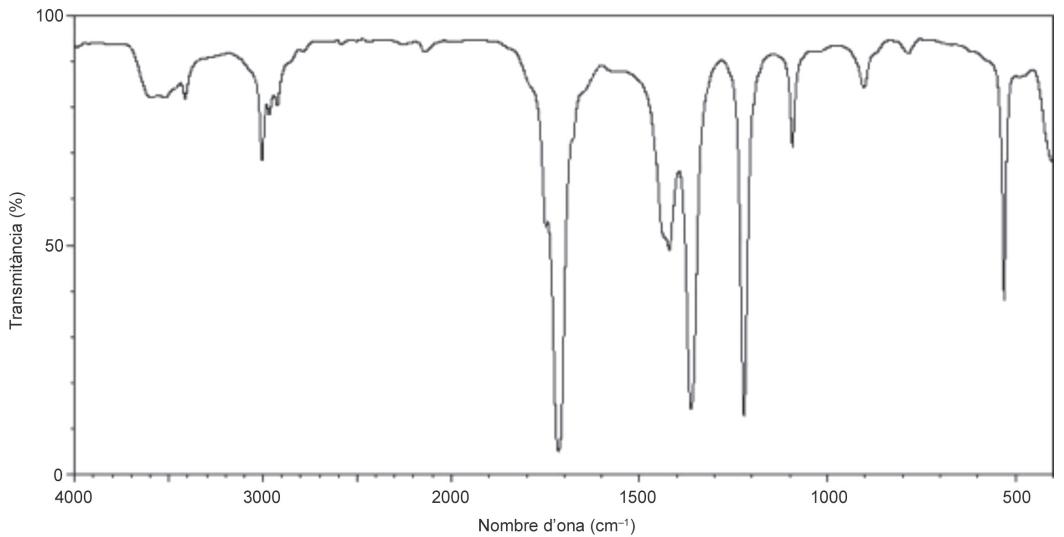
En el laboratorio, a una temperatura de , tenemos una muestra líquida que queremos etiquetar, pero no sabemos si se trata de la acetona o del propan-2-ol. Mediante un espectrofotómetro de infrarrojo obtenemos el gráfico siguiente para la muestra líquida:
Explique en qué se basa la espectroscopia infrarroja y qué representan los picos que se obtienen con esta técnica. A partir del gráfico anterior y de los datos de la tabla siguiente, indique a qué sustancia corresponde la muestra líquida y justifique la respuesta.
| Enlace | Tipo de compuesto | Intervalo de número de onda () |
| C-H | alcanos (C-C-H) | 2850-2970; 1340-1470 |
| alquenos (C=C-H) | 3010-3095; 675-995 | |
| O-H | alcoholes | 3200-3600 |
| ácidos carboxílicos | 2500-2700 | |
| C-O | alcoholes, éteres, ácidos carboxílicos, ésteres | 1050-1300 |
| C=O | aldehídos, cetonas, ácidos carboxílicos, ésteres | 1690-1760 |
Ejercicio 7 · Serie 4
7Serie 4
2 puntosSerie 4
Elija UNA cuestión de entre la 6 y la 7.
La electrólisis del agua se puede efectuar con un voltámetro de Hofmann, como se muestra en la figura:
En uno de los electrodos se obtiene oxígeno según la semirreacción siguiente:
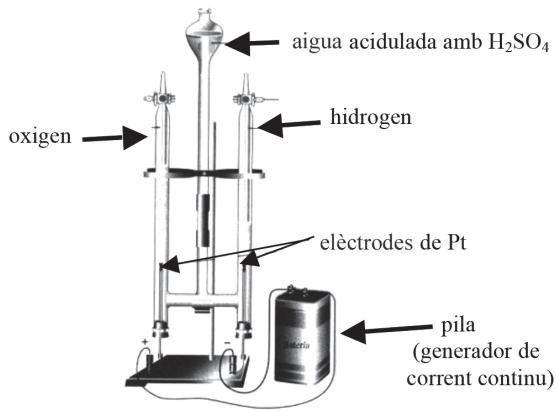
Escriba la semirreacción que tiene lugar en el otro electrodo e indique la polaridad de cada electrodo. ¿Qué gas se produce en el ánodo y cuál en el cátodo? ¿En todos los procesos electrolíticos es necesario suministrar energía mediante una pila? Justifique las respuestas.
El número de Avogadro (), que indica el número de partículas que contiene un mol de partículas, se puede obtener de manera experimental mediante una electrólisis. En el laboratorio hemos llevado a cabo una electrólisis de agua; hemos suministrado a la celda electrolítica una corriente eléctrica de durante y hemos obtenido de oxígeno, medidos a y . Calcule el número de Avogadro.
