3
2 puntosLa formación del es difícil de llevar a cabo experimentalmente porque, si no se utiliza un exceso de oxígeno, la reacción es incompleta, y si hay un exceso de oxígeno no se puede evitar que la oxidación continúe y se forme también . El valor de la entalpía de formación del gaseoso se calcula a partir de la determinación de las entalpías de combustión del grafito y del gaseoso.
Escribid la ecuación de la reacción de formación del gaseoso. Calculad la entalpía estándar de formación del gaseoso a partir de la figura siguiente:
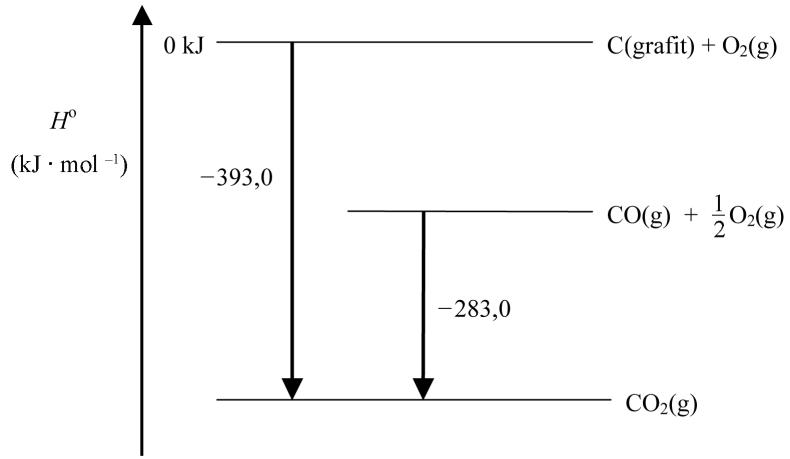
Se hacen reaccionar, a presión constante, de y de gaseoso medidos a y , y se forma gaseoso. ¿Qué cantidad de calor se desprende en esta reacción?
