¿Cuál es la constante de acidez del ácido fórmico a ?
QuímicaCataluñaPAU 2010Extraordinaria
Química · Cataluña 2010
7 ejercicios
Ejercicio 1
1
2 puntosSe prepara una solución acuosa de ácido fórmico, , mezclando de este ácido con agua en un vaso de precipitados. Después, la solución se trasvasa cuantitativamente a un matraz aforado de y se enrasa con agua. Se mide experimentalmente el pH de la solución a y se obtiene un valor de .
¿Cuál debería ser la concentración de una solución de ácido clorhídrico para que tuviera el mismo pH que la solución de ácido fórmico anterior?
Ejercicio 2
2
2 puntosA partir de soluciones de y , y empleando una solución de como puente salino, se construye en el laboratorio la pila siguiente, a una temperatura de :
| Par redox | ||
| (V), a |
Escribid las ecuaciones de las semirreacciones de oxidación y reducción, y la ecuación de la reacción iónica global de la pila. Calculad su fuerza electromotriz (FEM).
Dibujad un esquema de la pila. Indicad la polaridad y el nombre de cada electrodo y señalad en qué sentido se mueven los iones del puente salino.
Ejercicio 3
3
2 puntosLa formación del es difícil de llevar a cabo experimentalmente porque, si no se utiliza un exceso de oxígeno, la reacción es incompleta, y si hay un exceso de oxígeno no se puede evitar que la oxidación continúe y se forme también . El valor de la entalpía de formación del gaseoso se calcula a partir de la determinación de las entalpías de combustión del grafito y del gaseoso.
Escribid la ecuación de la reacción de formación del gaseoso. Calculad la entalpía estándar de formación del gaseoso a partir de la figura siguiente:
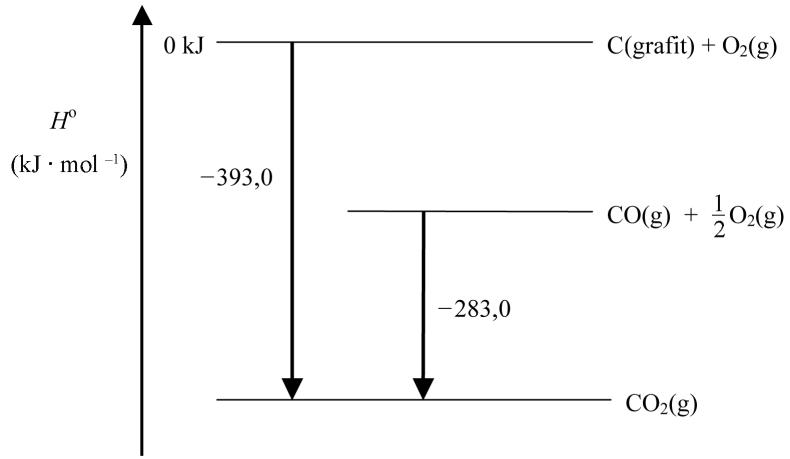
Se hacen reaccionar, a presión constante, de y de gaseoso medidos a y , y se forma gaseoso. ¿Qué cantidad de calor se desprende en esta reacción?
Ejercicio 4
4
2 puntosPara pasar un mol de moléculas de desde el nivel más bajo de vibración (estado fundamental) hasta el nivel de vibración siguiente se requiere una energía de .
Calculad la energía, expresada en J, que se necesita para pasar una molécula de desde el estado fundamental hasta el nivel de vibración siguiente. ¿Qué tipo de radiación electromagnética debería absorber una molécula de para realizar este proceso?
Calculad la frecuencia y la longitud de onda de la radiación electromagnética que debería absorber una molécula de para pasar del estado fundamental al nivel de vibración siguiente.
Ejercicio 5
5
2 puntosLa hidrólisis de la sacarosa, o azúcar de mesa, se puede efectuar en un medio ácido que actúa como catalizador. Se ha comprobado experimentalmente que esta reacción tiene una cinética de primer orden respecto de la sacarosa.
Definid el concepto de orden de reacción respecto de un reactivo. ¿Cuál de los siguientes gráficos (A, B o C) indica que la hidrólisis ácida de la sacarosa es de primer orden respecto de este reactivo? Razonad la respuesta.
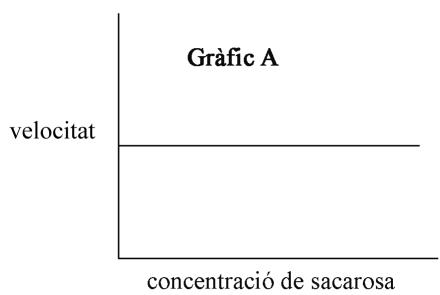
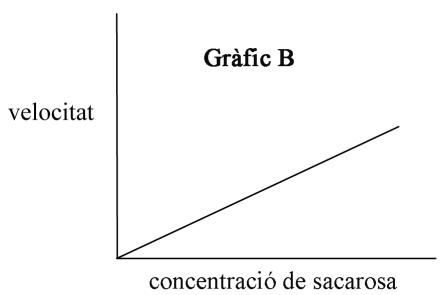
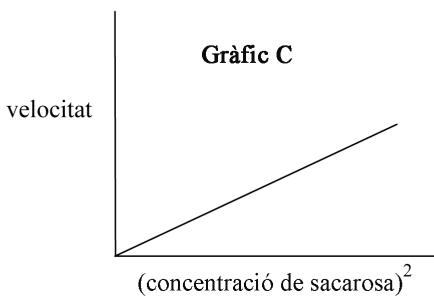
¿Qué es un catalizador? Explicad cómo actúa un catalizador en una reacción química a partir del modelo del estado de transición.
Ejercicio 6
6
2 puntosSe quiere efectuar un experimento en el laboratorio para determinar, de manera aproximada, la entalpía de disolución del hidróxido de potasio en agua.
Describid el procedimiento que seguiríais en el laboratorio y el material que usaríais.
Si al disolver de hidróxido de potasio en de agua se produce un incremento en la temperatura de la solución de , ¿cuál es la entalpía molar de la reacción de disolución del hidróxido de potasio?
Ejercicio 7
7
2 puntosEl proceso químico de oxidación de la glucosa transfiere energía al cuerpo humano:
En este proceso, a ; y
Determinad la energía libre que se obtiene, a , cuando tomamos una cucharada de glucosa (), suponiendo que las magnitudes y no varían con la temperatura.
¿Por qué esta reacción de oxidación de la glucosa, a , puede transferir energía al cuerpo humano?
