6
2,5 puntosLas energías reticulares de los compuestos iónicos son útiles para predecir los puntos de fusión y las solubilidades en agua de este tipo de compuestos. Para calcular el valor de la energía reticular de un compuesto iónico como el cloruro de rubidio, se utiliza el ciclo de Born-Haber.
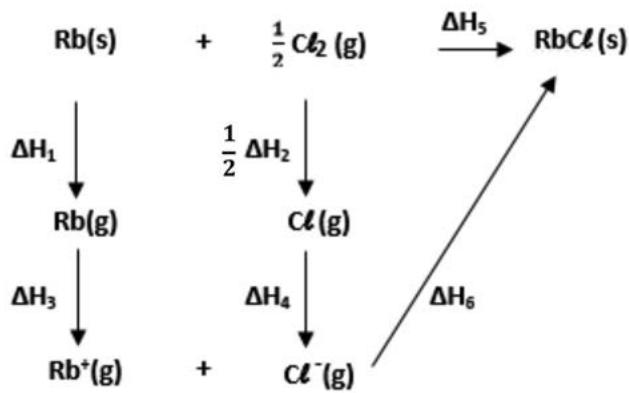
| 82 | 240 | 403 | -349 | -435 |
Escriba las reacciones correspondientes a la primera energía de ionización del rubidio, la afinidad electrónica del cloro y la entalpía de formación del cloruro de rubidio, e indique qué valor tienen las entalpías de cada uno de estos procesos. Diga si, según la configuración electrónica y el modelo atómico de cargas eléctricas, la primera energía de ionización del sodio será más grande o más pequeña que la del rubidio. Justifique la respuesta.
Calcule el valor de la energía reticular del cloruro de rubidio. Razone cualitativamente, según la configuración electrónica de cada elemento y el modelo atómico de cargas eléctricas, si la energía reticular del fluoruro de sodio () será más grande o más pequeña que la del cloruro de rubidio. Considere los valores absolutos de las energías reticulares.
