Se sabe que dos elementos, A y B, tienen los números atómicos (Z) 11 y 35, pero no se sabe a cuál corresponde cada uno. Escriba las configuraciones electrónicas de los elementos y y determine el grupo, el periodo y el bloque de los elementos de cada una de estas configuraciones. Sabemos que A y B forman el compuesto iónico AB y que es un compuesto covalente. ¿Qué número atómico corresponde a A y cuál corresponde a B? Justifique la respuesta de acuerdo con las propiedades del bloque al que pertenecen y las configuraciones electrónicas.
QuímicaCataluñaPAU 2024Ordinaria
Química · Cataluña 2024
7 ejercicios90 min de duración
Ejercicio 1
1
2,5 puntosLa tabla periódica ordena los elementos químicos de número atómico más pequeño a más grande. Se organiza en siete periodos (filas), dieciocho grupos o familias (columnas) y cuatro bloques, según las configuraciones electrónicas (bloques s, p, d y f).
Los rayos X y la radiación gamma son calificados de radiaciones ionizantes porque pueden provocar mutaciones y originar la formación de especies activas en los tejidos de los seres vivos. Tienen longitudes de onda () comprendidas entre y m. Defina el término energía de ionización de un elemento y razone qué signo tiene. Sabiendo que la energía de ionización del hidrógeno es de , ¿se podría ionizar el átomo de hidrógeno con una radiación de longitud de onda de ?
Ejercicio 2
2
2,5 puntosEl ácido glucónico () es un ácido orgánico monoprótico que se utiliza como aditivo alimentario (E 574) para corregir la acidez. El control del pH de los alimentos también tiene un efecto como conservante, ya que cuando el pH de un alimento es inferior a se puede evitar el crecimiento de bacterias nocivas para la salud de las personas.
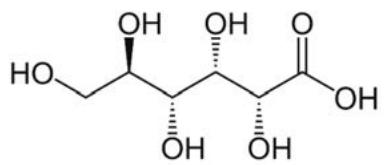
Determine las concentraciones en el equilibrio de todas las especies de una muestra que contiene de ácido glucónico en de solución acuosa. Razone si en esta muestra podrán crecer o no las bacterias nocivas.
Esta solución se valora con hidróxido de sodio. Escriba la reacción de valoración y justifique cualitativamente si el valor del pH en el punto de equivalencia es ácido, básico o neutro. Haga un dibujo del montaje experimental y enumere todo el material de laboratorio y otras sustancias necesarias para poder llevar a cabo la valoración.
Ejercicio 3
3
2,5 puntosLa glucosa () es un monosacárido que se encuentra en muchos alimentos y en la sangre. En la fabricación del pan es muy importante la reacción de fermentación de la glucosa por acción de la levadura. En esta reacción de fermentación se obtiene etanol () y dióxido de carbono ().
Calcule la entalpía estándar de la reacción de fermentación de la glucosa a a partir de las reacciones de combustión de la glucosa y de combustión del etanol, si sabemos que la combustión de de glucosa desprende a y la combustión de de etanol desprende a . ¿La reacción de fermentación de la glucosa es endotérmica o exotérmica? Justifique la respuesta.
La glucosa es una de las principales fuentes de energía para el cuerpo humano. Determine de cuánta energía de Gibbs estándar a se dispone para mantener la actividad muscular y nerviosa del cuerpo a partir de la combustión de de glucosa en condiciones fisiológicas (la temperatura de la sangre en condiciones normales es de ). ¿Se trata de una reacción espontánea en condiciones fisiológicas? Justifique la respuesta. Considere que la entalpía y la entropía estándar no varían con la temperatura.
| Sustancia | ||||
| 213,8 | 205,2 | 70,0 | 2121,0 |
Ejercicio 4
4
2,5 puntosEl acetato de etilo (también llamado etanoato de etilo) es un disolvente orgánico utilizado ampliamente en diferentes sectores industriales. Se obtiene principalmente mediante la reacción de esterificación de Fisher a partir de ácido acético y etanol, en presencia de un catalizador ácido y calor:
Se hacen reaccionar de etanol con de ácido acético. Cuando la reacción llega al equilibrio quedan de ácido acético sin reaccionar. Determine el valor de la constante de equilibrio () de la reacción. Considere que el volumen de la mezcla líquida de reacción se mantiene constante durante el proceso. Indique qué representan cada uno de los pictogramas del ácido acético y el etanol, y qué problemas pueden causar.

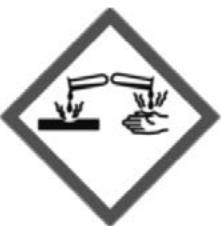


Para conseguir el máximo rendimiento en un proceso industrial de obtención de acetato de etilo, se utilizan principalmente dos estrategias: realizar la reacción con un gran exceso de etanol y eliminar el agua del recipiente de reacción. Razone por qué estas dos estrategias hacen aumentar el rendimiento de la reacción. Explique qué efecto tendría sobre el rendimiento de la reacción el hecho de no utilizar un catalizador.
Ejercicio 5
5
2,5 puntosEn el laboratorio disponemos de láminas de plata y cobre, así como de dos soluciones acuosas de concentración , una de sal de nitrato de plata () y la otra de sal de nitrato de cobre(II) (). También disponemos del material para hacer un puente salino.
Haga el dibujo de la pila que se podría montar con los electrodos de cobre y plata, indicando todo el material necesario. Indique cuál de los electrodos de la pila funciona como ánodo y cuál como cátodo, su polaridad y la dirección en que circulan los electrones por el circuito externo. Escriba las semirreacciones y la reacción global.
Considerando la pila del apartado anterior, calcule la fuerza electromotriz estándar a y escriba la notación esquemática de la pila. Argumente si la lámina de cobre que actúa como electrodo aumenta o disminuye de masa a medida que avanza la reacción.
Ejercicio 6
6
2,5 puntosLas energías reticulares de los compuestos iónicos son útiles para predecir los puntos de fusión y las solubilidades en agua de este tipo de compuestos. Para calcular el valor de la energía reticular de un compuesto iónico como el cloruro de rubidio, se utiliza el ciclo de Born-Haber.
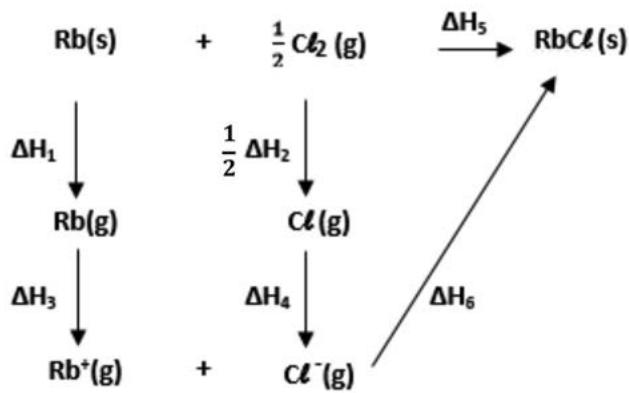
| 82 | 240 | 403 | -349 | -435 |
Escriba las reacciones correspondientes a la primera energía de ionización del rubidio, la afinidad electrónica del cloro y la entalpía de formación del cloruro de rubidio, e indique qué valor tienen las entalpías de cada uno de estos procesos. Diga si, según la configuración electrónica y el modelo atómico de cargas eléctricas, la primera energía de ionización del sodio será más grande o más pequeña que la del rubidio. Justifique la respuesta.
Calcule el valor de la energía reticular del cloruro de rubidio. Razone cualitativamente, según la configuración electrónica de cada elemento y el modelo atómico de cargas eléctricas, si la energía reticular del fluoruro de sodio () será más grande o más pequeña que la del cloruro de rubidio. Considere los valores absolutos de las energías reticulares.
Ejercicio 7
7
2,5 puntosEl infrarrojo es la parte del espectro electromagnético comprendida entre las regiones visible y de microondas. Es una radiación poco energética que solo provoca cambios en los niveles de energía vibracional de los enlaces de las moléculas. Es la técnica espectroscópica ideal para identificar rápidamente los tipos de grupos funcionales presentes en un determinado compuesto orgánico o material.
Rodee y nombre todos los grupos funcionales de las moléculas A, B y C que se indican a continuación. Dibuje las tres moléculas A, B y C añadiendo los pares de electrones no compartidos en los heteroátomos (átomos que no son C ni H).
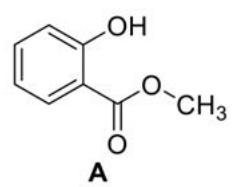
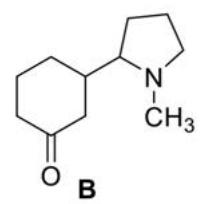
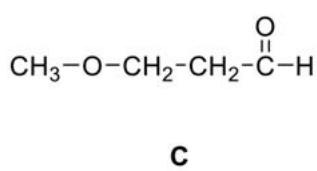
A continuación se muestra el espectro de infrarrojo de una de las moléculas (A, B o C) del apartado anterior. Razone a cuál de las tres moléculas pertenece el espectro. Indique qué señal o señales del espectro le permiten identificar la molécula y qué señales serían comunes en las tres moléculas.
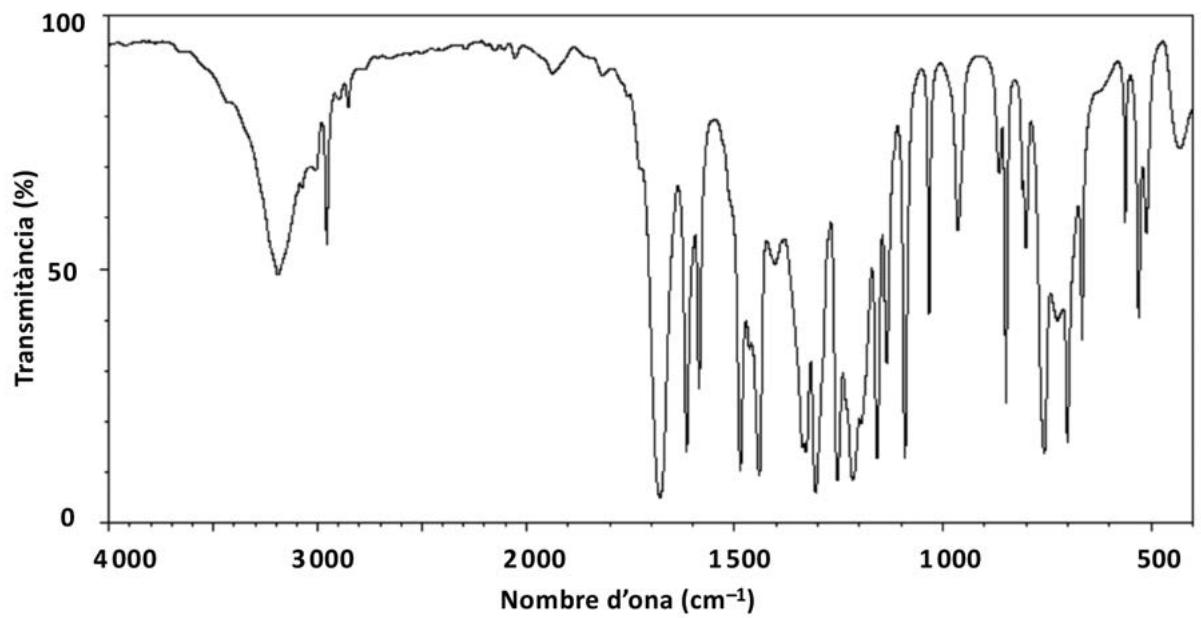
| Datos espectroscópicos en la región del infrarrojo | |
| Enlace | Intervalo del número de onda () |
| C—H | 2850-3000 |
| O—H | 3550-3200 |
| C=C | 1500-1650 |
| C=O | 1650-1750 |
| C—O | 1000-1300 |
| C—N | 1100-1250 |
