3
2,5 puntosLa cal viva es el óxido de calcio que se obtiene de la calcinación de rocas calizas. La cal apagada es hidróxido de calcio que se produce por hidratación del óxido de calcio en un proceso exotérmico. Ambas sustancias tienen múltiples aplicaciones en diversos ámbitos, pero sobre todo se utilizan en la construcción para obtener mortero y yeso.
Calculad el calor que se desprende en la reacción de hidratación de la cal viva. Justificad que la reacción es exotérmica. ¿Qué cantidad de calor se liberará a presión constante en el proceso de hidratación de una tonelada () de cal viva?
| Sustancia | CaO(s) | H2O(l) | Ca(OH)2(s) |
| Entalpía estándar de formación a 298 K (kJ mol-1) | -634,9 | -285,5 | -985,6 |
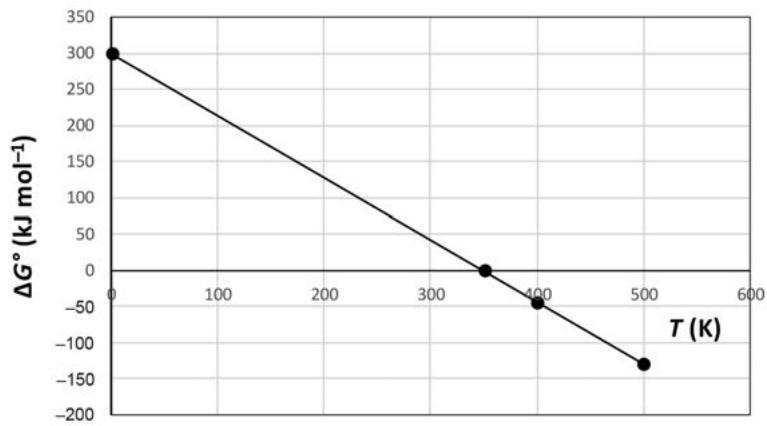
El gráfico siguiente representa la variación con la temperatura de la energía de Gibbs de una determinada reacción. Considerando que la variación de entalpía y de entropía de la reacción son constantes en todo el intervalo de temperaturas del gráfico, y considerando la reacción en condiciones estándar, razonad a qué temperatura la reacción se encontrará en condiciones de equilibrio. Determinad el valor de la variación de entalpía estándar de la reacción, indicad si será endotérmica o exotérmica y justificad la respuesta. Razonad a partir de qué temperatura la reacción será espontánea.