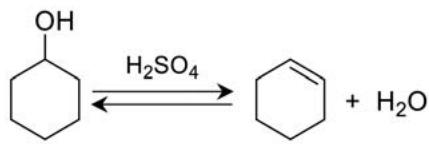
Escribid las reacciones del ácido láctico con el agua y del ion lactato con agua. Indicad, para cada reacción, según la teoría de Brønsted y Lowry, qué especies actúan de ácido y base, y cuáles son los respectivos ácidos y bases conjugados. Razonad si el pH de una solución de lactato de sodio es ácido, básico o neutro, y cómo podríamos distinguir esta solución de una solución de ácido láctico mediante un papel indicador universal.
| Cambio de color de un papel indicador universal en función del pH | |||||
| Color | Rojo | Amarillo | Verde | Azul | Azul muy oscuro |
| Intervalo del pH | 0-3 | 4-5 | 6-7 | 8-10 | 11-14 |