3
2 puntosEl peróxido de hidrógeno (agua oxigenada) es un producto de desecho de muchas de las reacciones que tienen lugar en las células vivas. La enzima catalasa provoca su descomposición en productos menos nocivos:
Se puede investigar experimentalmente la cinética de esta reacción midiendo la cantidad de oxígeno gaseoso que se produce con el paso del tiempo. En una primera serie de experimentos en el laboratorio se obtuvieron los datos que se muestran en la tabla siguiente:
| Experimento | inicial () | Velocidad inicial () |
| 1 | 0,10 | 4,2 |
| 2 | 0,20 | 8,5 |
| 3 | 0,30 | 12,7 |
| 4 | 0,40 | 16,8 |
Justifique cuál es el orden de reacción respecto al peróxido de hidrógeno y calcule la constante de velocidad de la reacción.
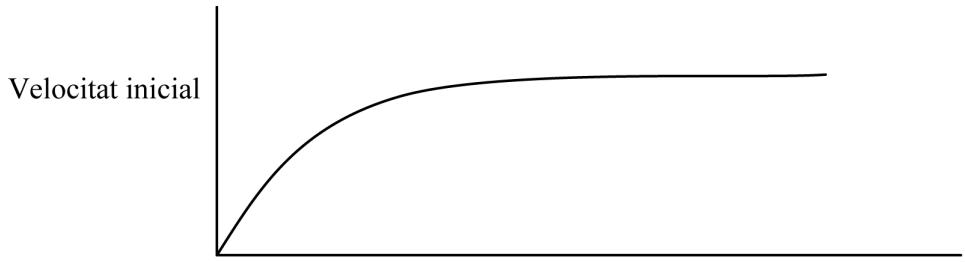
Si llevamos a cabo una segunda serie de experimentos en el laboratorio, similar a la anterior pero utilizando un conjunto de soluciones de peróxido de hidrógeno de concentraciones más elevadas, obtenemos la representación gráfica siguiente. Justifique cuál es el orden de reacción respecto al peróxido de hidrógeno a concentraciones elevadas. Escriba la ecuación de velocidad en estas condiciones e indique las unidades de la constante de velocidad.