Calcule su solubilidad en agua a , y exprésela en .
QuímicaCataluñaPAU 2011Extraordinaria
Química · Cataluña 2011
7 ejercicios
Ejercicio 1
1
2 puntosEl hidróxido de magnesio, , es una sustancia que se utiliza en pequeñas cantidades como antiácido y también como laxante.
Sin cambiar la temperatura, explique razonadamente cómo variará la solubilidad del hidróxido de magnesio si, en vez de disolverlo en agua, lo disolvemos en una solución de nitrato de magnesio. ¿Y si lo disolvemos en una solución de ácido clorhídrico?
Ejercicio 2
2
2 puntosEl ácido sulfúrico es uno de los compuestos más fabricados del mundo. Actualmente, la mayor parte de la producción se utiliza para elaborar fertilizantes, aunque también se utiliza en diversos procesos metalúrgicos o en las baterías de los automóviles. Una de las etapas en el proceso de obtención del ácido sulfúrico es la reacción de oxidación del dióxido de azufre a trióxido de azufre. A partir de los datos de la tabla siguiente, responda a las cuestiones y justifique las respuestas.
| Reacción: | |||
| Temperatura (K) | 500 | 700 | 1100 |
| Constante de equilibrio en presiones () | |||
¿Para conseguir que la reacción tenga un rendimiento alto, conviene trabajar a temperaturas altas o bajas?
¿En qué condiciones de presión podemos mejorar el rendimiento de la reacción?
Ejercicio 3
3
2 puntosEl peróxido de hidrógeno (agua oxigenada) es un producto de desecho de muchas de las reacciones que tienen lugar en las células vivas. La enzima catalasa provoca su descomposición en productos menos nocivos:
Se puede investigar experimentalmente la cinética de esta reacción midiendo la cantidad de oxígeno gaseoso que se produce con el paso del tiempo. En una primera serie de experimentos en el laboratorio se obtuvieron los datos que se muestran en la tabla siguiente:
| Experimento | inicial () | Velocidad inicial () |
| 1 | 0,10 | 4,2 |
| 2 | 0,20 | 8,5 |
| 3 | 0,30 | 12,7 |
| 4 | 0,40 | 16,8 |
Justifique cuál es el orden de reacción respecto al peróxido de hidrógeno y calcule la constante de velocidad de la reacción.
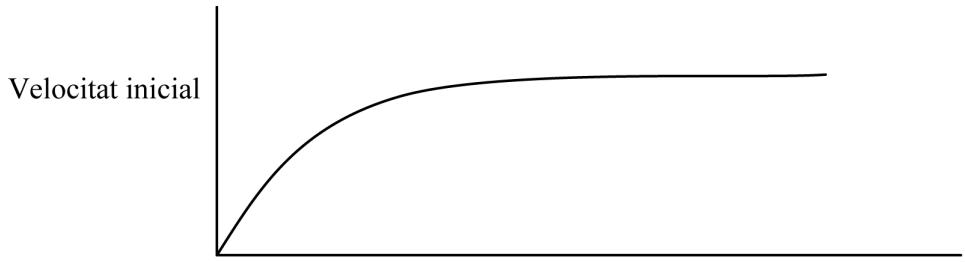
Si llevamos a cabo una segunda serie de experimentos en el laboratorio, similar a la anterior pero utilizando un conjunto de soluciones de peróxido de hidrógeno de concentraciones más elevadas, obtenemos la representación gráfica siguiente. Justifique cuál es el orden de reacción respecto al peróxido de hidrógeno a concentraciones elevadas. Escriba la ecuación de velocidad en estas condiciones e indique las unidades de la constante de velocidad.
Ejercicio 4
4
2 puntosElija entre la cuestión 4 y la 5.
Dos elementos tienen las configuraciones electrónicas siguientes en el estado fundamental:
La primera energía de ionización de uno de los elementos es , mientras que la del otro es .
¿Cuál de los dos elementos tiene un radio atómico más grande? Asigne los valores de la primera energía de ionización a cada uno de los elementos, X e Y. Justifique las respuestas utilizando el modelo atómico de cargas eléctricas.
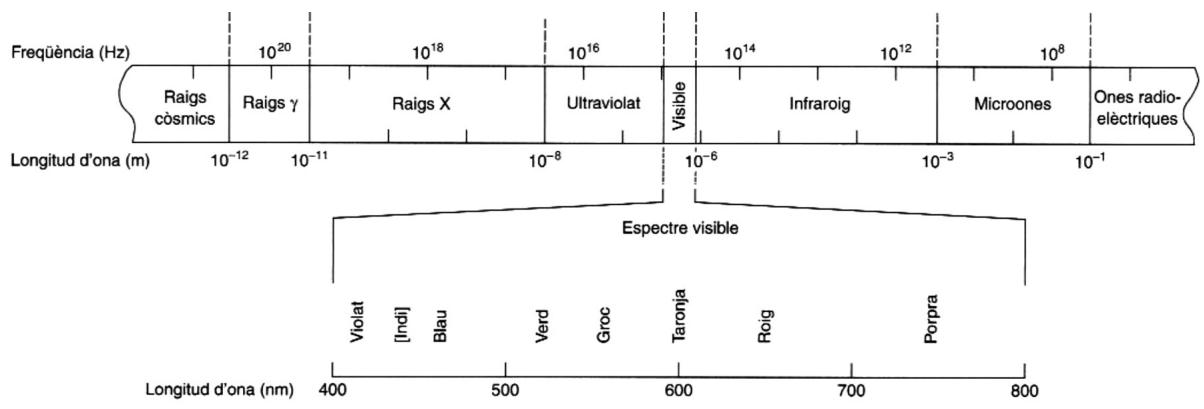
Indique, a partir de la figura siguiente, qué tipo de radiación electromagnética habría que utilizar para provocar la ionización del elemento que tiene la primera energía de ionización de .
Ejercicio 5
5
2 puntosElija entre la cuestión 4 y la 5.
Queremos determinar la entalpía de reacción de una solución acuosa de con una solución acuosa de :
Explique el procedimiento experimental que seguiría en el laboratorio, e indique el material que utilizaría y las medidas experimentales que habría que determinar para poder calcular la entalpía de reacción.
Calcule el calor desprendido cuando se mezclan de con de , si experimentalmente hemos determinado que la entalpía de la reacción anterior es .
Ejercicio 6
6
2 puntosElija entre la cuestión 6 y la 7.
Aunque los cubiertos de plata se oscurecen por la reacción con los compuestos sulfurados que contienen los alimentos, es corriente recubrir de plata cubiertos fabricados con otros metales más baratos. Queremos recubrir de plata una cuchara mediante el proceso electrolítico de una solución acuosa de una sal de plata.
Justifique si la cuchara debe actuar como ánodo o como cátodo de la celda electrolítica. Haga un dibujo esquemático de este proceso electrolítico: indique el nombre y la polaridad de los electrodos y la reacción que tendrá lugar en el electrodo donde está la cuchara.
Determine cuántas horas se necesitan para llevar a cabo el recubrimiento, si la cuchara tiene una superficie de , el espesor del recubrimiento debe ser de y por el baño utilizado pasa una corriente de .
Ejercicio 7
7
2 puntosElija entre la cuestión 6 y la 7.
Hay una gran variedad de productos comerciales para limpiar y desinfectar las instalaciones de ordeño de ganado. Incluso se puede utilizar, con esta finalidad, una solución acuosa de hidróxido de sodio preparada con la disolución de de este hidróxido en agua destilada, hasta obtener de solución.
Calcule el pH de esta solución de limpieza de hidróxido de sodio, a .
Se valora la solución de limpieza de hidróxido de sodio con una solución acuosa de , utilizando un sensor de pH. Escriba la reacción de valoración, haga un dibujo aproximado de la curva de valoración e indique dónde se encuentra el punto de equivalencia. Justifique cuál es el pH en este punto de equivalencia.
