1Opción A
1 puntoEl vinagre es una disolución acuosa de ácido acético () en la que hay como mínimo g de ácido por cada mL de vinagre. La Oficina del Consumidor decide analizar un vinagre comercial para ver si cumple las especificaciones requeridas. Se toma una muestra de mL de vinagre y se valora con una disolución acuosa de hidróxido de sodio () M. En la figura 1 se han representado los valores de pH en función del volumen de añadido.
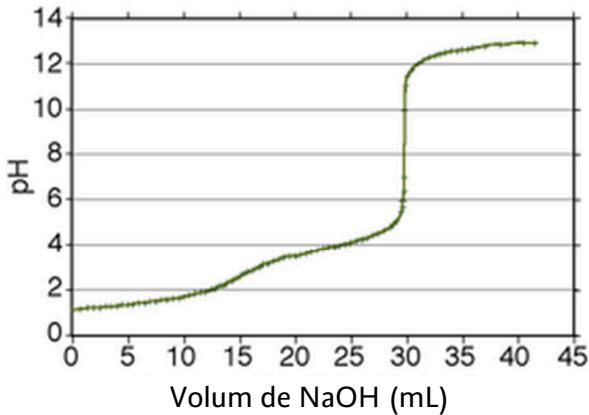
Di, haciendo los cálculos pertinentes, si este vinagre cumple las normas vigentes.
¿Cuál de los indicadores de la tabla 1 sería el más adecuado para determinar el punto de equivalencia de la valoración anterior? Razona la respuesta.
| Indicador | Zona de viraje |
| Violeta de metilo | 0,1-1,5 |
| Azul de bromofenol | 3,0-4,6 |
| Azul de timol | 8,0-9,8 |
