Di, haciendo los cálculos pertinentes, si este vinagre cumple las normas vigentes.
QuímicaBalearesPAU 2017Ordinaria
Química · Baleares 2017
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
1 puntoEl vinagre es una disolución acuosa de ácido acético () en la que hay como mínimo g de ácido por cada mL de vinagre. La Oficina del Consumidor decide analizar un vinagre comercial para ver si cumple las especificaciones requeridas. Se toma una muestra de mL de vinagre y se valora con una disolución acuosa de hidróxido de sodio () M. En la figura 1 se han representado los valores de pH en función del volumen de añadido.
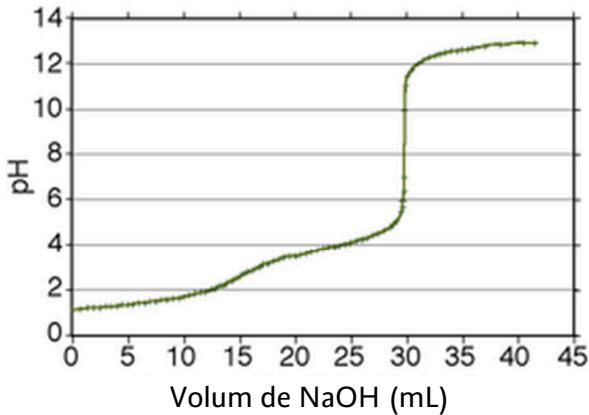
¿Cuál de los indicadores de la tabla 1 sería el más adecuado para determinar el punto de equivalencia de la valoración anterior? Razona la respuesta.
| Indicador | Zona de viraje |
| Violeta de metilo | 0,1-1,5 |
| Azul de bromofenol | 3,0-4,6 |
| Azul de timol | 8,0-9,8 |
Ejercicio 1 · Opción B
1Opción B
2,5 puntosEl se descompone según la reacción siguiente:
En un recipiente cerrado y vacío de L se introducen g de a K. Una vez el sistema ha alcanzado el equilibrio químico a K, se comprueba que la presión total es de atm.
Determina el grado de disociación del .
Calcula el valor de a K.
¿Cómo afectaría al equilibrio químico un aumento de la temperatura? ¿Y la adición de un catalizador? Razona la respuesta.
Ejercicio 2 · Opción A
2Opción A
2 puntosEl producto de solubilidad del es de a ºC.
Determina la solubilidad del en agua a ºC en unidades g/mL.
Indica razonadamente si precipitará cuando se mezclan mL de M con mL de M.
Ejercicio 2 · Opción B
2Opción B
2 puntosSe mezclan mL de ácido nítrico () M con mL de M. Suponiendo que los volúmenes son aditivos, determina el pH de la disolución resultante.
¿Cuál será el volumen de M que se necesita para neutralizar mL de una disolución M de ? Razona la respuesta.
¿Es cierto que una disolución de es ácida? Razona la respuesta.
Ejercicio 3 · Opción A
3Opción A
2 puntosLa reacción de descomposición del propanal viene dada por:
Y su ecuación de velocidad es:
Se ha comprobado en el laboratorio que cuando la concentración inicial de propanal es de , la velocidad inicial de reacción es .
Calcula el valor de la constante de velocidad, , de la reacción.
¿Es correcto suponer que la velocidad de reacción () es independiente de la temperatura? Razona la respuesta.
Formula y nombra un isómero funcional del propanal.
Ejercicio 3 · Opción B
3Opción B
2 puntosSe construye una pila galvánica formada por un electrodo de sumergido en una disolución de , y un electrodo de sumergido en una disolución de .
Indica la reacción que tendrá lugar en el ánodo.
Determina el potencial de la pila.
Además de los electrodos de , y de un voltímetro, ¿qué otros dos elementos son necesarios para el montaje de la pila galvánica? Indica su función.
Ejercicio 4 · Opción A
4Opción A
2,5 puntosSean los elementos , y .
Escribe la configuración electrónica del ion más estable del .
¿Cuál de los tres elementos presenta mayor radio atómico? Razona la respuesta.
¿Cuál de los tres elementos presenta mayor electronegatividad? Razona la respuesta.
Explica el tipo de enlace en las siguientes moléculas: y .
Ejercicio 4 · Opción B
4Opción B
2 puntosLos puntos de fusión de dos sustancias son ºC y ºC. Indica, de manera justificada, qué punto de fusión corresponde al y cuál a la sílice ().
Justifica la geometría de la molécula de y la hibridación del átomo de carbono.
Ejercicio 5 · Opción A
5Opción A
2,5 puntosSea la siguiente reacción no ajustada:
Ajusta la reacción iónica por el método del ion-electrón.
¿Cuál es la especie oxidante? Razona la respuesta.
Nombra los compuestos siguientes: y .
Ejercicio 5 · Opción B
5Opción B
1,5 puntosFormula o nombra los compuestos siguientes: 3-metil-2-butanol, y .
En la ficha de seguridad química del aparece el pictograma siguiente. Indica su significado.

