El premio Nobel de Química del año 2018 fue concedido a los investigadores Frances H. Arnold, George P. Smith y Sir Gregory P. Winter (figura 1), por el descubrimiento de un nuevo método usado en la ingeniería de proteínas, el cual imita el proceso de selección natural con el propósito de dirigir las proteínas hacia un objetivo definido.
La treonina (figura 2) es uno de los aminoácidos esenciales utilizados por estos investigadores.

A partir de la estructura química de la treonina (figura 2), determina su masa molecular.
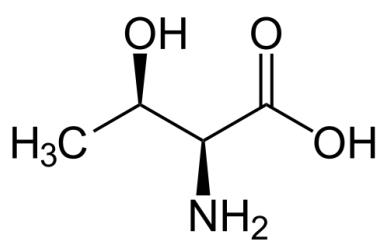
Nombra dos grupos funcionales presentes en la molécula de la treonina.

