La presión total que ejercerían los gases liberados si la temperatura del recipiente es de .
QuímicaComunidad ValencianaPAU 2023Extraordinaria
Química · Comunidad Valenciana 2023
10 ejercicios
Ejercicio 1 · Bloque I
1Bloque I
2 puntosBloque I
El nitrato de amonio, , es una sal que se utiliza como fertilizante, aunque, bajo ciertas condiciones, se descompone explosivamente según la ecuación química siguiente no ajustada:
Un bidón de contiene de una sustancia que tiene un de riqueza en nitrato de amonio. Si se calienta y llegase a explotar totalmente, calcule:
¿Qué volumen de agua se obtendría?
Ejercicio 1 · Bloque II
1Bloque II
2 puntosBloque II
Responda a las siguientes cuestiones sobre estructura atómica y propiedades periódicas:
Escriba las configuraciones electrónicas de los iones , y e identifique el número de grupo y periodo al que pertenecen los elementos correspondientes.
Compare razonadamente el radio atómico del yodo, , con el radio iónico del yoduro, .
Ordene de menor a mayor la primera energía de ionización de los siguientes elementos: , y . Razone la respuesta.
Ejercicio 2 · Bloque I
2Bloque I
2 puntosBloque I
El dióxido de carbono, , reacciona con carbono, , para dar monóxido de carbono, , de acuerdo con el equilibrio:
En un reactor de de volumen, mantenido a , en el que se ha hecho previamente el vacío, se introduce hasta que la presión en su interior alcanza y, posteriormente, se añade un exceso de carbono. Una vez alcanzado el equilibrio la presión en el interior del reactor es de .
Calcule las constantes y del equilibrio plantejado.
Si tras vaciar completamente el reactor, se introduce únicamente hasta alcanzar una presión de , calcule la masa (en gramos) de cada uno de los tres componentes de la mezcla una vez se alcance el equilibrio.
Ejercicio 2 · Bloque II
2Bloque II
2 puntosBloque II
Responda a las siguientes cuestiones sobre estructura molecular y estructuras de Lewis:
Dibuje la estructura electrónica de Lewis de las siguientes especies químicas: disulfuro de carbono , dióxido de azufre , sulfuro de hidrógeno y formaldehído .
Indique la hibridación de los átomos de de las moléculas y .
Deduzca la geometría molecular de y .
Deduzca cuál de los dos ángulos es mayor: o bien en las moléculas de y , respectivamente.
Ejercicio 3 · Bloque I
3Bloque I
2 puntosBloque I
El ácido glicólico es un ácido monoprótico, , que se utiliza por los dermatólogos para desvanecer arrugas y disminuir el acné debido a su carácter irritante. El efecto que produce en la piel depende de la concentración utilizada; de hecho, sólo los dermatólogos pueden utilizar disoluciones con pH por debajo de 3.
Si la constante de acidez, , del ácido glicólico es de , calcule la concentración de ácido que tendrá que utilizar un dermatólogo para que el pH de la disolución que va a utilizar en un tratamiento sea de 2.
Si el dermatólogo toma de la disolución anterior y añade agua hasta un volumen total de , ¿qué pH tendrá ahora la nueva disolución de ácido glicólico?
Ejercicio 3 · Bloque II
3Bloque II
2 puntosBloque II
El amoníaco, , se obtiene industrialmente partir de dihidrógeno, , y dinitrógeno, , de acuerdo con el equilibrio:
Discuta razonadamente cómo afectará cada uno de los cambios introducidos a la cantidad de presente en el reactor una vez se restablezca el equilibrio:
Adicionar al sistema en equilibrio, manteniendo constantes la temperatura y el volumen.
Reducir el volumen del reactor a la meitat, manteniendo constante la temperatura.
Añadir al reactor un número de moles de , y tal que se dupliquen las concentraciones que había en el equilibrio, manteniendo constantes la temperatura y el volumen.
Aumentar la temperatura del reactor.
Ejercicio 4 · Bloque I
4Bloque I
2 puntosBloque I
En el departamento de calidad de una industria se desea determinar el porcentaje de hierro en un alambre. Para ello, se disuelve, en medio ácido, un trozo de alambre que pesa , obteniéndose finalmente de una disolución de (ac). Se tratan de esta disolución con una disolución de dicromato de potasio , necesitando para la reacción completa del (ac), de acuerdo con la ecuación química siguiente no ajustada:
Identifique justificadamente el agente oxidante y el reductor. Ajuste la ecuación química.
Calcule el porcentaje de hierro en el alambre.
Ejercicio 4 · Bloque II
4Bloque II
2 puntosBloque II
Teniendo en cuenta los potenciales estándar de reducción, responda razonadamente si los siguientes enunciados son verdaderos o falsos:
Una barra de estaño es estable cuando se introduce en una disolución acuosa de .
Al sumergir una barra de hierro en una disolución acuosa de , se recubre con cromo.
El aluminio se disuelve en una disolución acuosa de .
Las disoluciones acuosas de se pueden guardar en recipientes de aluminio.
Ejercicio 5
5
2 puntosBloque II
La ley de velocidad para la reacción es . Justifique si las siguientes afirmaciones son verdaderas o falsas:
El reactivo se consume más deprisa que el .
La velocidad de la reacción aumentará el doble al disminuir el volumen a la mitad.
Las unidades de la constante de velocidad son .
Al aumentar la temperatura aumenta la velocidad de reacción.
Ejercicio 6
6
2 puntosBloque II
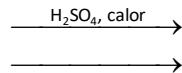
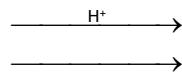
Complete las siguientes reacciones, nombre los compuestos orgánicos en ellas involucrados e indique el tipo de reacción de que se trata en cada caso: