Calcule el pH de esta solución a .
QuímicaCataluñaPAU 2010Ordinaria
Química · Cataluña 2010
14 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosEl gas amoníaco, , es uno de los compuestos más fabricados del mundo. La gran importancia que tiene se debe a la facilidad con que se puede convertir en otros productos que contienen nitrógeno. En el ámbito doméstico, encontramos soluciones de amoníaco en una amplia variedad de productos de limpieza. Suponga que preparamos en el laboratorio una solución acuosa de amoníaco de concentración inicial :
Razone si una solución acuosa de será ácida, neutra o básica.
Ejercicio 1 · Opción B
1Opción B
2 puntosEn los motores de los automóviles se produce la reacción siguiente, que provoca contaminación atmosférica por óxidos de nitrogeno:
La constante de equilibrio de concentraciones de esta reacción es a , pero a una temperatura de es .
Razone si la reacción es endotérmica o exotérmica.
Si en un recipiente cerrado de de volumen que está a una temperatura de introducimos de nitrógeno y de oxígeno, ¿cuántos moles de monóxido de nitrógeno habrá en el recipiente cuando la reacción alcance el equilibrio?
Ejercicio 2 · Opción A
2Opción A
2 puntosEl dióxido de nitrógeno se puede formar a partir del monóxido de nitrógeno, a , según la reacción siguiente:
| Temperatura = 298 K | NO(g) | O2(g) | NO2(g) |
| (J·K⁻¹·mol⁻¹) | 210,8 | 205,1 | 240,1 |
Razone si la reacción será espontánea en condiciones estándar y a .
Calcule el calor a presión constante que se desprenderá al reaccionar de monóxido de nitrógeno, medidos a y , con un exceso de oxígeno.
Ejercicio 2 · Opción B
2Opción B
2 puntosAl realizar la electrólisis de cloruro de litio fundido, , se obtiene en el ánodo y en el cátodo.
Escriba el proceso que tiene lugar en cada uno de los electrodos e indique cuál es el proceso de oxidación y cuál el de reducción. ¿Qué polaridad tienen los electrodos?
Calcule la intensidad de corriente necesaria para descomponer de cloruro de litio fundido en una hora.
Ejercicio 3 · Opción A
3Opción A
2 puntosCon la ayuda de esta gráfica, en la que se muestra la energía de ionización de los sesenta primeros elementos de la tabla periódica, responda a las cuestiones siguientes:
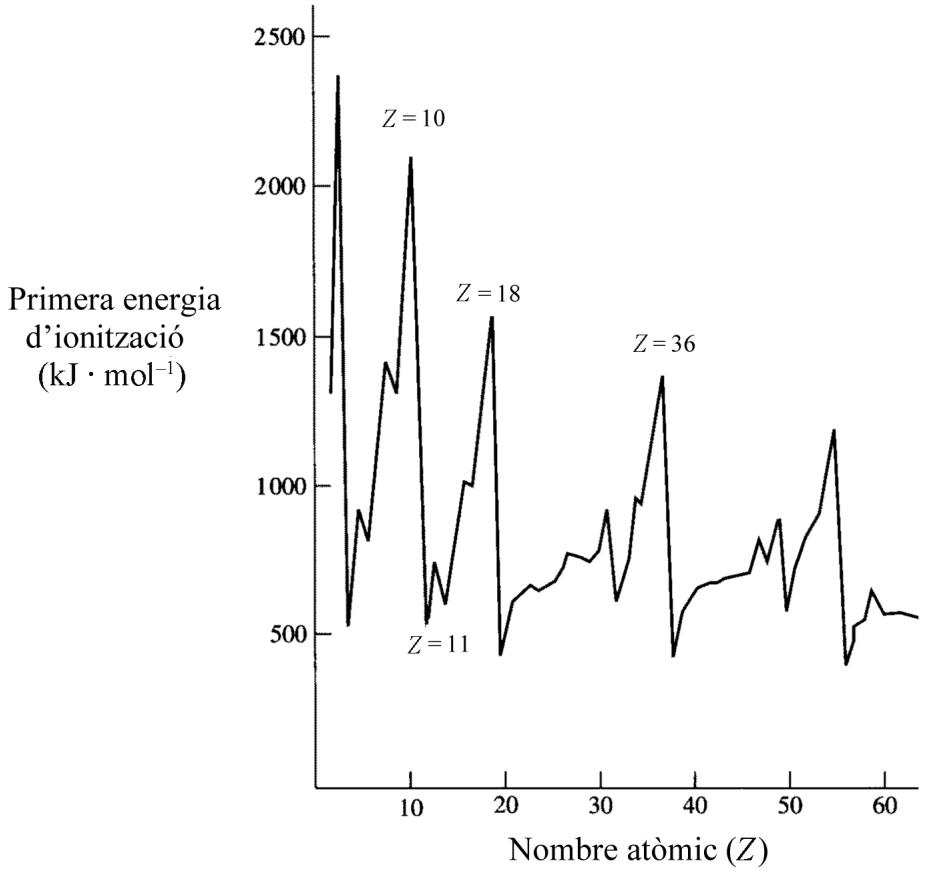
Defina el concepto de energía de ionización de un elemento. Justifique, a partir de la estructura electrónica de los átomos, por qué la primera energía de ionización es tan alta en los elementos situados en los picos de la figura.
Compare la energía de ionización del sodio () con la del magnesio () y justifique sus valores según las estructuras electrónicas de estos dos elementos.
Ejercicio 3 · Opción B
3Opción B
2 puntosEl carbonato de calcio se descompone, en condiciones estándar y a , según la reacción siguiente:
Si la entropía estándar de esta reacción () es :
Calcule la energía libre estándar de la reacción a . Razone si la reacción es espontánea en condiciones estándar y a .
¿Qué temperatura mínima se debe alcanzar para que el sólido se descomponga en condiciones estándar? Considere que y no varían con la temperatura.
Ejercicio 4 · Opción A
4Opción A
2 puntosElija UNA cuestión entre la 4 y la 5.
En el laboratorio disponemos de una solución acuosa de , de una solución acuosa de y de hierro y aluminio sólidos.
| Temperatura = 25 °C | Cu2+/Cu | Fe2+/Fe | Zn2+/Zn | Al3+/Al |
| (V) | +0,34 | -0,44 | -0,76 | -1,68 |
¿Qué reacción haría para obtener zinc sólido? Justifique la respuesta.
Escriba la ecuación de la reacción entre la solución acuosa de y el aluminio sólido y calcule la energía libre estándar de esta reacción.
Ejercicio 4 · Opción B
4Opción B
2 puntosElija UNA cuestión entre la 4 y la 5.
Queremos obtener la curva de valoración de de una solución acuosa de ácido clorhídrico con una solución acuosa de hidróxido de sodio .
Explique el procedimiento experimental que seguiría en el laboratorio e indique el material que usaría para obtener la curva de valoración.
Escriba la reacción de valoración, realice un dibujo aproximado de la curva de valoración y señale en ella el punto de equivalencia. Razone qué pH tendrá la valoración en este punto a .
Ejercicio 5 · Opción A
5Opción A
2 puntosElija UNA cuestión entre la 4 y la 5.
Mediante el proceso de electrólisis del agua se pueden obtener hidrógeno y oxígeno gaseosos.
Indique el material que necesitaría para llevar a cabo este proceso en el laboratorio y realice un esquema del montaje experimental. Escriba las ecuaciones de las semirreacciones que tienen lugar en cada uno de los electrodos.
Determine el volumen de hidrógeno, medido a y , que se obtendrá al efectuar la electrólisis del agua durante media hora con una intensidad de corriente de .
Ejercicio 5 · Opción B
5Opción B
2 puntosElija UNA cuestión entre la 4 y la 5.
La reacción de combustión del metano, a y , se produce según la ecuación siguiente:
En la combustión del metano, ¿es mayor la cantidad de energía implicada en la rotura de enlaces o en la formación de enlaces? Razone la respuesta.
Calcule la entalpía del enlace C−H.
| Enlace | O=O | C=O | O-H |
| Entalpía de enlace (kJ·mol⁻¹) | 498 | 805 | 464 |
Ejercicio 6 · Opción A
6Opción A
2 puntosElija UNA cuestión entre la 6 y la 7.
El dióxido de carbono, uno de los gases de la atmósfera, absorbe parte de la radiación infrarroja emitida por la superficie de la Tierra.
Explique qué le sucede a la molécula de dióxido de carbono cuando absorbe un fotón de radiación infrarroja. ¿Por qué las moléculas de dióxido de carbono absorben solo ciertas frecuencias de radiación infrarroja?
Calcule la frecuencia y la longitud de onda de un fotón de radiación infrarroja que tiene una energía de .
Ejercicio 6 · Opción B
6Opción B
2 puntosElija UNA cuestión entre la 6 y la 7.
La figura siguiente muestra el radio atómico de los cuarenta y cinco primeros elementos de la tabla periódica:
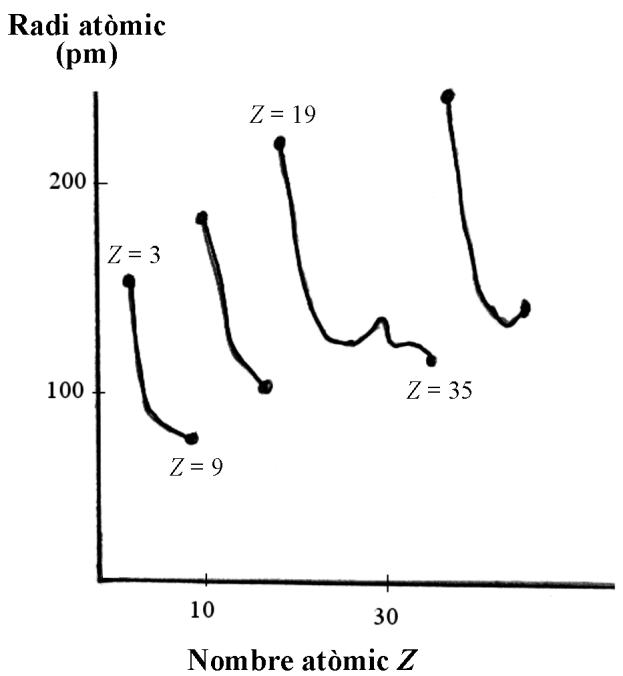
Justifique, a partir de la estructura electrónica de los átomos, la variación del radio atómico a lo largo del segundo periodo de la tabla periódica (números atómicos del 3 al 9).
Compare el radio atómico del litio () y el del potasio () y justifique estos valores a partir de la estructura electrónica de los dos átomos.
Ejercicio 7 · Opción A
7Opción A
2 puntosElija UNA cuestión entre la 6 y la 7.
La figura siguiente muestra el diagrama de la cinética de la reacción .
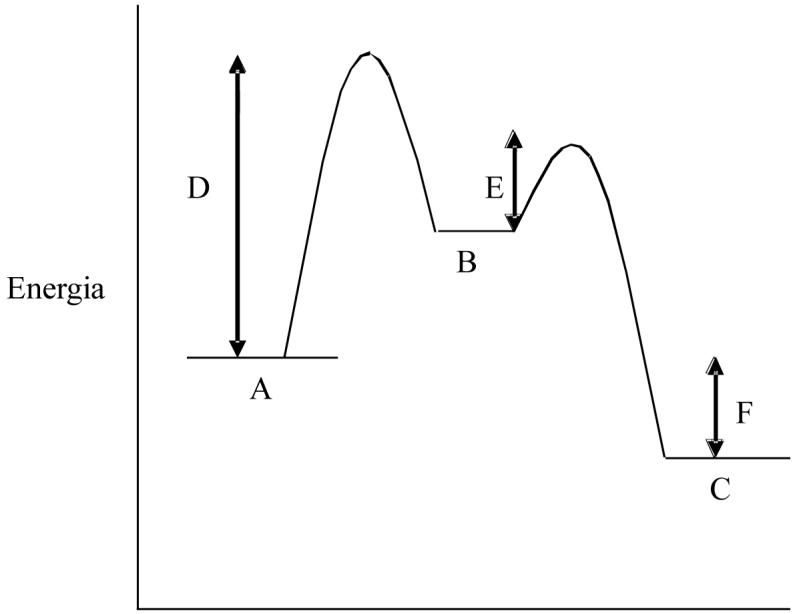
Razone si se trata de una reacción elemental o de una reacción que incluye etapas. ¿Qué representa B? ¿Qué magnitudes representan D y E?
¿Es una reacción endotérmica o exotérmica? ¿Se modificarían D y F si la reacción se produjera en presencia de un catalizador? Justifique las respuestas.
Ejercicio 7 · Opción B
7Opción B
2 puntosElija UNA cuestión entre la 6 y la 7.
Una radiación electromagnética se puede definir mediante cualquiera de los parámetros siguientes: energía, longitud de onda, frecuencia o número de onda.
Aplicamos a una determinada molécula las radiaciones electromagnéticas que se indican en la tabla siguiente. Ordénelas de más a menos energía y justifique la respuesta.
| Radiación | radiación 1 | radiación 2 | radiación 3 |
| Valor y unidad | 2,65·10⁻¹⁷ J | 2,70·10⁻⁷ m | 5,10·10¹⁴ s⁻¹ |
Las moléculas de ozono () de la estratosfera absorben ciertas radiaciones ultravioletas y ayudan a proteger a los seres humanos de padecer cáncer de piel. Por otro lado, las moléculas de dióxido de carbono () de la troposfera absorben ciertas radiaciones infrarrojas emitidas por la superficie de la Tierra y provocan el calentamiento de la atmósfera por el efecto invernadero. Explique qué tipos de cambios se producen en las moléculas de ozono y de dióxido de carbono en estos procesos de absorción de radiación electromagnética.
