Calcule las presiones parciales de todos los componentes en dicho equilibrio.
QuímicaAragónPAU 2025Ordinaria
Química · Aragón 2025
5 ejercicios
Ejercicio 1
1
2 puntosLos óxidos de nitrógeno () son una familia de compuestos gaseosos formados en procesos de combustión a altas temperaturas, como en motores diésel, plantas industriales y centrales eléctricas. Los más comunes son el y el . En el aire, los reaccionan con otros compuestos y forman smog fotoquímico, una niebla contaminante que dificulta la respiración y afecta especialmente a personas con asma o problemas pulmonares. También contribuyen a la lluvia ácida, que daña suelos, bosques, ríos y edificios. Además, los ayudan a la formación de ozono en la parte baja de la atmósfera, un gas que, aunque en la capa de ozono es beneficioso, a nivel del suelo es tóxico para los seres vivos y perjudica el crecimiento de las plantas.
Los compuestos reductores, como el amoniaco o el Adblue (disolución acuosa de urea) usado en vehículos diésel, descomponen los en componentes menos dañinos, como el nitrógeno y el vapor de agua, reduciendo así las emisiones ambientales.
El hidrógeno molecular () se está estudiando como agente reductor alternativo para la eliminación de , ya que ofrece ventajas como que puede funcionar a temperaturas más bajas que otros métodos y, si el hidrógeno proviene de fuentes renovables, ayuda a reducir aún más la contaminación. Esto lo convierte en una alternativa prometedora para hacer que los motores y las industrias sean más limpias y respetuosas con el medio ambiente. En una prueba utilizando este último método de eliminación de , se introdujeron en un recipiente un mol de monóxido de nitrógeno y otro mol de dihidrógeno, y se calentaron hasta , alcanzándose el siguiente equilibrio:
En el equilibrio, la presión total fue de y el grado de disociación del fue .

Calcule los valores de y para ese equilibrio a .
Ejercicio 2
2
2 puntosCalcule el pH de una disolución de ácido hipocloroso (). ()
Calcule el pH de la disolución obtenida al añadir de una disolución de a de una disolución de . Considere los volúmenes aditivos.
Ejercicio 3
3
2 puntosResponda solo a uno de estos dos apartados (3D o 3E).
Responda razonadamente a las siguientes cuestiones teniendo en cuenta la tabla periódica que se muestra en la figura y los elementos situados en ella.
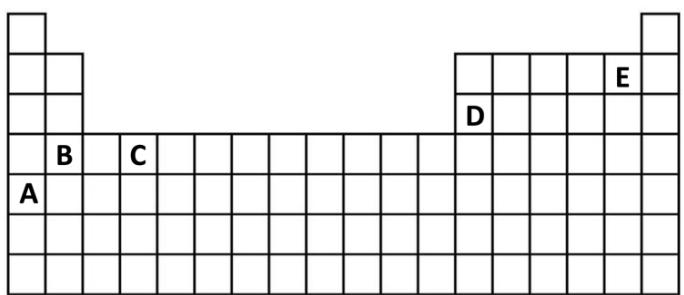
Escriba la configuración electrónica de los elementos A y C, e indique de qué elementos se trata.
Ordene de menor a mayor electronegatividad los elementos (A, B, C, D y E) representados en la tabla.
¿Qué elemento (A, B, C, D o E) será el de mayor radio atómico? ¿Y el que tenga una mayor afinidad electrónica?
¿Cuál será el ion más probable que formará el elemento B? Compare razonadamente el radio del átomo B neutro con el de su ion.
Indique las posibles combinaciones de números cuánticos que podría tener el electrón más energético del elemento D.
Ejercicio 4
4
2 puntosResponda solo a uno de estos dos apartados (4A o 4B).
4A) Resuelva las siguientes cuestiones sobre solubilidad:
Datos
- Masas atómicas:
Se adicionan de en de agua a , ¿se disolverá todo el sólido?
¿La expresión del producto de solubilidad del es Razone la respuesta.
En una disolución saturada de , la es , ¿cuál es la solubilidad molar del
4B) Dada la reacción: , se sabe que es de primer orden respecto al reactivo A y de segundo orden respecto al reactivo B. Responda las siguientes cuestiones justificando cada respuesta:
a) Escriba la expresión de la ecuación de velocidad de esta reacción. Determine cuál es el orden global de la reacción.
b) Si el volumen del reactor se reduce manteniendo la temperatura constante, ¿qué ocurrirá con la velocidad de la reacción?
c) Si la temperatura del sistema aumenta, ¿qué efecto tendrá sobre la velocidad de reacción?
d) ¿Cómo afectará a la velocidad de reacción la adición de un catalizador? ¿El catalizador influirá en la cantidad de productos obtenidos?
Ejercicio 5
5
2 puntosResponda solo a uno de estos dos apartados (5A o 5B).
5A) Justifique si los siguientes procesos redox son espontáneos o no en condiciones estándar. En cada caso ajuste la ecuación e identifique al oxidante y al reductor.
a)
b)
c)
d)
Datos
5B) La reacción de disociación del es la siguiente:
a) Calcule la entalpía molar estándar del proceso y razone si la reacción de disociación del es una reacción endotérmica o exotérmica.
b) Calcule la variación de entropía de la reacción y razone si en la reacción de disociación del disminuye o aumenta el desorden.
c) Justifique si la reacción de disociación del en condiciones estándar () es una reacción espontánea.
Datos
