un solo electrón descrito por un orbital p;
QuímicaAsturiasPAU 2023Extraordinaria
Química · Asturias 2023
10 ejercicios
Ejercicio 1
1
2 puntosEscriba la configuración electrónica completa del elemento de número atómico más bajo que, en su estado fundamental, tenga:
una subcapa p completa;
dos electrones descritos por orbitales 3p;
tres electrones descritos por orbitales 4p.
Ejercicio 2
2
2 puntosLa gráfica muestra los valores experimentales de la primera energía de ionización, , de los ocho elementos que forman el tercer periodo de la tabla periódica (, , , , , , y ).
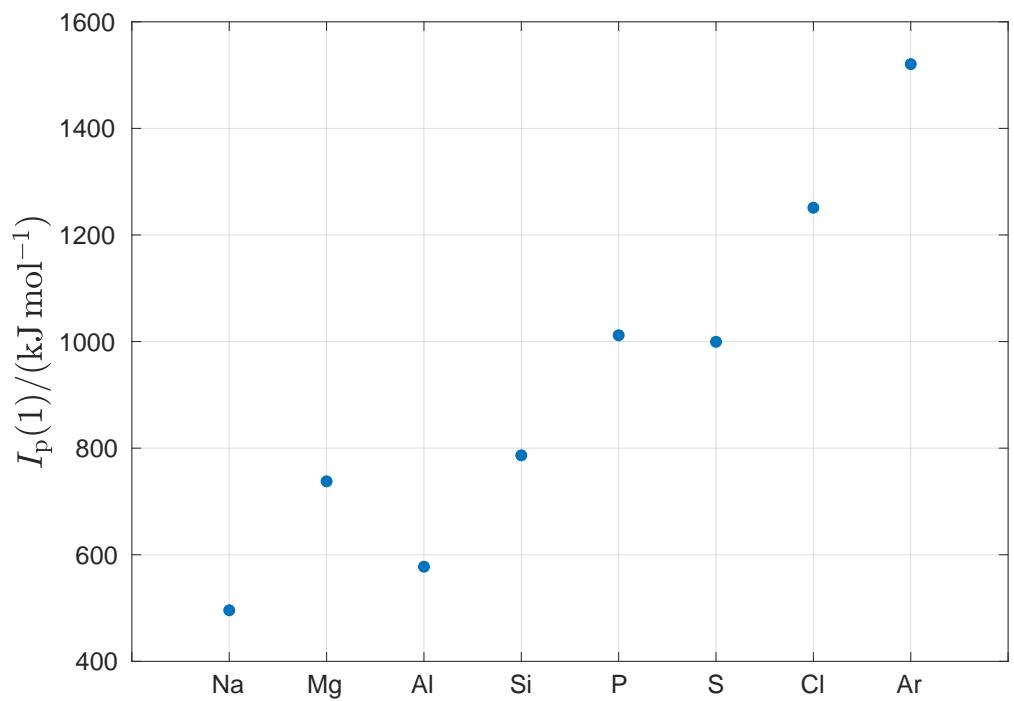
Indique a qué es debida la tendencia general observada.
Justifique las excepciones encontradas (Mg y P).
Ejercicio 3
3
2 puntosLa constante de equilibrio para la reacción a , es (cuando las presiones se expresan en atm). En un recipiente de , a , se introducen de . Calcule las presiones parciales del y del cuando se alcanza el estado de equilibrio.
Ejercicio 4
4
2 puntosLa reacción es de primer orden en ambos reactivos.
Si y , . Calcule el valor de .
Calcule cuando y .
Calcule cuando y la concentración de es tres veces la de .
Ejercicio 5
5
2 puntosCalcule, a , el pH de una disolución acuosa de ().
Ejercicio 6
6
2 puntosEl hipoclorito de sodio, , reacciona con el hidróxido de cromo(III), , en presencia de hidróxido sódico, , generándose, entre otras especies, los aniones cloruro, , y cromato, .
Identifique el elemento que se reduce y sus estados de oxidación inicial y final.
Escriba la semirreacción de reducción, en forma iónica, ajustada en medio básico.
Identifique el elemento que se oxida y sus estados de oxidación inicial y final.
Escriba la semirreacción de oxidación, en forma iónica, ajustada en medio básico.
Escriba la reacción de oxidación-reducción, en forma iónica, ajustada.
Escriba la reacción de oxidación-reducción, en forma molecular, ajustada.
Ejercicio 7
7
2 puntosEscriba el nombre del material de laboratorio utilizado en la realización de una volumetría ácido-base.
Escriba la expresión de la constante de equilibrio ( o ) de los siguientes procesos:
Ejercicio 8
8
2 puntosEscriba el procedimiento experimental seguido en la realización de una volumetría ácido-base.
de una disolución acuosa de peróxido de hidrógeno, , se valora, en medio ácido (), con una disolución acuosa de permanganato potásico, , . Calcule la masa de que hay en la disolución acuosa original sabiendo que, después de añadirle de la disolución acuosa de , adquiere un color púrpura pálido.
Ejercicio 9
9
2 puntosSe muestran, a continuación, las fórmulas estructurales semidesarrolladas del eteno y del etino. Justifique, utilizando los esquemas de hibridación de la teoría del enlace de valencia (TEV), los valores aproximados que toman los ángulos y .
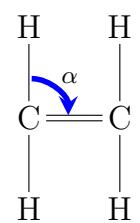
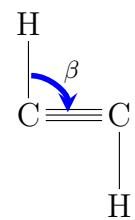
Escriba la fórmula estructural semidesarrollada de los siguientes compuestos: butano, propeno, propan-1-ol, ciclohexeno, 3-metilbut-1-eno y clorometanol.
Ejercicio 10
10
2 puntosUtilice los datos de la tabla para calcular el número de electrones desapareados que existen en los estados fundamentales de los iones y .
| 3 | 8 |
¿Qué nombre recibe el compuesto que se forma al hacer reaccionar propan-2-ol con una disolución acuosa ácida de dicromato de potasio, ?
Escriba la fórmula estructural semidesarrollada de dicho compuesto.
¿Qué tipo de reacción ha tenido lugar?
