Indique el electrodo que actúa como ánodo y el que actúa como cátodo en la celda. Escriba las reacciones que tienen lugar en el ánodo y en el cátodo de la célula electrolítica. Justifique las respuestas.
QuímicaAsturiasPAU 2015Ordinaria
Química · Asturias 2015
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2,5 puntosConstruya el ciclo de Born-Haber para la formación del , a partir de yodo sólido y sodio metálico, y calcule la energía de red del compuesto, a partir de los siguientes datos:
Ejercicio 1 · Opción B
1Opción B
2,5 puntosDetermine si se formará precipitado cuando se mezclan de agua destilada con de disolución acuosa de nitrato de bario, , y con de disolución acuosa de carbonato de sodio, , . Suponga que los volúmenes son aditivos.
Ejercicio 2 · Opción A
2Opción A
2,5 puntosEl oro se suele depositar sobre otros metales menos caros mediante electrolisis, dando lugar a la joyería de objetos bañados en oro. La reacción electrolítica en la superficie donde se deposita el oro es:
En la celda electrolítica, el objeto que se baña con oro es uno de los electrodos y el otro es una lámina de oro.
Cuando se hace pasar una corriente de durante minutos, se depositan de oro. Calcule el rendimiento del proceso electrolítico.
Ejercicio 2 · Opción B
2Opción B
2,5 puntosLa neutralización exacta de de una disolución acuosa de ácido cianhídrico, , consumió de disolución acuosa de hidróxido de sodio, , . Calcule el pH de la disolución acuosa de ácido cianhídrico.
Ejercicio 3 · Opción A
3Opción A
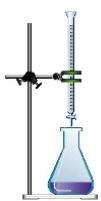
1 puntoEn el laboratorio se dispone del dispositivo experimental de la figura y del material de laboratorio y reactivos que se relaciona: pipeta aforada de , disolución acuosa titulada de , muestra de vinagre comercial e indicador.
Indique el procedimiento experimental a seguir para realizar la determinación del contenido de ácido acético en un vinagre comercial.
Ejercicio 3 · Opción B
3Opción B
1 puntoDibuje un esquema de la pila Daniell e indique el material de laboratorio y los reactivos utilizados para su construcción.
Ejercicio 4 · Opción A
4Opción A
2 puntosOrdene las siguientes especies de acuerdo con el valor creciente de su radio: , , . Justifique la respuesta.
Para el anión , deduzca la estructura de Lewis. Nombre y dibuje la geometría molecular e indique los ángulos de enlace aproximados.
Datos
Ejercicio 4 · Opción B
4Opción B
2 puntosLas siguientes configuraciones electrónicas:
i) ;
ii) .
representan estados excitados de los átomos. Para cada caso escriba la configuración electrónica del estado fundamental e indique el grupo de la tabla periódica al que pertenece cada elemento.
Para las sustancias: y , indique, de forma razonada, las fuerzas intermoleculares presentes en cada una de ellas y la sustancia que presentará el punto de ebullición más bajo.
Ejercicio 5 · Opción A
5Opción A
2 puntosCalcule los moles de carbonato de calcio sólido, , que se obtienen al evaporar a sequedad de una disolución acuosa saturada de carbonato de calcio.
Datos
Escriba las fórmulas semidesarrolladas y nombre los isómeros geométricos del 2-penteno.
Ejercicio 5 · Opción B
5Opción B
2 puntosLas entalpías estándar de formación de los óxidos y , a partir de y oxígeno gaseoso, son y , respectivamente. A partir de estos datos, calcule la entalpía estándar de la reacción:
Escriba las fórmulas semidesarrolladas de los siguientes compuestos:
i. 2,4,9-trimetildecano
ii. Butanal
iii. 3-pentanona
iv. Acetato de metilo
