Indique, de forma razonada, el sentido en el que el sistema evolucionará de forma espontánea para alcanzar el estado de equilibrio.
QuímicaAsturiasPAU 2020Ordinaria
Química · Asturias 2020
10 ejercicios90 min de duración
Ejercicio 1 · Opción A
1Opción A
2 puntosEn un recipiente cerrado de , en el que inicialmente se ha realizado el vacío, se introducen moles de pentacloruro de fósforo, , moles de tricloruro de fósforo, y moles de cloro, , y se eleva la temperatura de la mezcla gaseosa a , alcanzándose el siguiente equilibrio:
Calcule la concentración en el equilibrio del .
Ejercicio 1 · Opción B
1Opción B
2 puntosEn de una disolución acuosa saturada de sulfato de calcio, , a , hay de disuelto. Calcule el valor de la constante del producto de solubilidad del en agua a .
Ejercicio 2 · Opción A
2Opción A
2 puntosCalcule el pH de la disolución resultante de diluir de una disolución acuosa de etilamina, , de concentración con agua hasta un volumen final de la disolución de .
Ejercicio 2 · Opción B
2Opción B
2 puntosAl añadir permanganato de potasio, , a una disolución acuosa de ácido clorhídrico, , se produce una reacción química de oxidación-reducción espontánea, dando lugar a cloruro de manganeso (II), , y se observa la liberación de cloro, .
Indique, de forma razonada, la especie química en disolución que experimenta la reacción de oxidación y la que experimenta la reacción de reducción.
Escriba y ajuste por el método del ion-electrón, en forma iónica, la ecuación que representa la reacción química que se produce de forma espontánea.
Calcule el potencial estándar de la reacción global.
Ejercicio 3 · Opción A
3Opción A
2 puntosLa determinación de la concentración de peróxido de hidrógeno, , en un agua oxigenada puede llevarse a cabo mediante la valoración denominada permanganimetría, de acuerdo con la siguiente ecuación química:
Enumere el material de laboratorio necesario para realizar la determinación de la concentración de en el agua oxigenada comercial, utilizando una disolución de permanganato de potasio. Indique dónde se alojaría la disolución acuosa de permanganato potásico.
Se toman de agua oxigenada y se diluyen con agua hasta un volumen final de . La valoración exacta de esta disolución consume, en el punto de equivalencia, de una disolución acuosa de permanganato de potasio . Calcule la concentración de peróxido de hidrógeno en el agua oxigenada inicial, expresando el resultado en gramos de por disolución.
Ejercicio 3 · Opción B
3Opción B
2 puntosEn la realización de una volumetría ácido-base para determinar la concentración de ácido acético () en un vinagre comercial, empleando hidróxido de sodio () como reactivo valorante, del vinagre se diluyen con de agua. La neutralización exacta de esta disolución consume de una disolución acuosa de hidróxido de sodio, , .
Calcule la concentración de ácido acético en el vinagre comercial e indique donde colocaría la disolución acuosa de para realizar la valoración.
Proponga, de forma razonada, cuál de los indicadores que aparecen recogidos en la siguiente tabla utilizaría para identificar el punto de equivalencia, indicando el cambio de color que se observaría, e indique el nombre del material en donde colocaría el indicador durante la realización de la valoración.
| Indicador | Color (medio ácido) | Color (medio básico) | Intervalo de pH de cambio de color |
| Amarillo de metilo | Rojo | Amarillo | 2,0-4,0 |
| Verde de bromocresol | Amarillo | Azul | 4,0-5,6 |
| Rojo de fenol | Amarillo | Rojo | 6,8-8,4 |
Ejercicio 4 · Opción A
4Opción A
2 puntosPara el anión nitrito, , deduzca la estructura de Lewis. Indique y dibuje la geometría molecular del compuesto, según la TRPECV, y los ángulos de enlace aproximados.
Datos
Escriba las configuraciones electrónicas, en estado fundamental, de los elementos () e (). Indique el bloque y periodo de la tabla periódica a los que pertenece cada uno de los elementos. A partir de su posición en la tabla periódica, indique, de forma razonada, el elemento que previsiblemente presentará el valor más negativo de la afinidad electrónica.
Ejercicio 4 · Opción B
4Opción B
2 puntosEscriba la configuración electrónica e indique el número de electrones desapareados para cada una de las siguientes especies: (); (); (); ().
Las temperaturas de ebullición a la presión de de las sustancias y son y , respectivamente. Justifique la diferencia en los valores de las temperaturas de ebullición de estas dos sustancias.
Datos
- Valores de la electronegatividad:
Ejercicio 5 · Opción A
5Opción A
2 puntosDe los siguientes conjuntos de números cuánticos indique, justificando la respuesta, el que representa correctamente a un electrón en un átomo: i) ii)
Identifique y nombre los grupos funcionales presentes en los siguientes compuestos:
i) Ver imagen.
ii)
iii) Ver imagen.
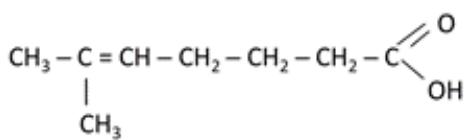
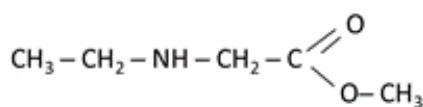
Ejercicio 5 · Opción B
5Opción B
2 puntosPara el indique, razonadamente, el número de protones y de neutrones que hay en el núcleo del átomo.
Escriba las fórmulas semidesarrolladas de los siguientes compuestos:
i) 1,4-dibromobenceno (p-dibromobenceno)
ii) Ácido 3,3-diclorohexanoico
iii) 3-metil-3-pentanol (3-metilpentan-3-ol)
iv) 2-pentanona (pentan-2-ona)
v) cis-2,3-dibromo-2-penteno (cis-2,3-dibromopent-2-eno)
vi) etildimetilamina
