Calcula los grados de disociación () de dos disoluciones acuosas de cada ácido y exprésalos en tanto por ciento. Indica qué ácido se disocia más.
QuímicaPaís VascoPAU 2023Extraordinaria
Química · País Vasco 2023
10 ejercicios90 min de duración
Datos generales del examen
- Masas atómicas (uma):
- Números atómicos: ()
- ()
- ()
- ()
- ()
- ()
- ()
- ()
Ejercicio 1 · Opción A
1Opción A
2,5 puntosA
Los ácidos metanoico () y etanoico () son débiles y sus respectivas constantes de ionización son: y
Calcula la concentración de ácido etanoico en una disolución acuosa para que su pH sea igual al de un ácido metanoico . Indica dicho pH.
Ejercicio 1 · Opción B
1Opción B
2 puntosB
La concentración del ión plata de una disolución saturada de sulfato de plata () es de . Calcula:
La concentración de ión sulfato en dicha disolución y el producto de solubilidad del sulfato de plata.
¿Se formará un precipitado de sulfato de plata al mezclar de nitrato de plata (aq) y de sulfato de sodio (aq) ?. Razona la respuesta.
Ejercicio 1 · Opción C
1Opción C
1,5 puntosC
Dada la ecuación química:
Indica qué átomos se oxidan o se reducen y los cambios que experimentan sus estados de oxidación.
Escribe la ecuación molecular ajustada por el método del ión-electrón.
Ejercicio 2 · Opción A
2Opción A
2,5 puntosA
El disulfuro de carbono () y el hidrógeno reaccionan a según la ecuación:
Se introducen de y de en un recipiente de y se calienta la mezcla a . Si la presión total tras alcanzar el equilibrio es de :
¿Cuántos moles de metano () se formarán tras alcanzar el equilibrio?
Calcula la constante de equilibrio a .
Justifica cómo cambiará la concentración de metano en el equilibrio al disminuir la presión.
Ejercicio 2 · Opción B
2Opción B
2 puntosB
Estos son los componentes de una pila electroquímica:
Electrodos metálicos: plata y magnesio
Electrólitos: nitrato de magnesio(II) (aq) y nitrato de plata (aq)
Puente salino: nitrato potásico (aq)
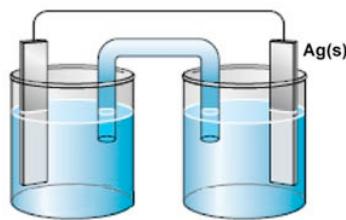
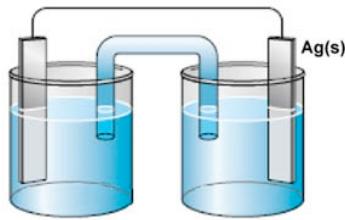
Completa la figura de la pila y asigna cada componente a una semipila.
Indica qué electrodo actuará como cátodo.
Escribe la ecuación química del proceso que ocurre en el ánodo.
Indica el sentido de la corriente de electrones en el hilo metálico.
Indica hacia dónde se mueven los iones del puente salino.
Ejercicio 2 · Opción C
2Opción C
1,5 puntosC
Dada la fórmula molecular .
Dibuja y nombra las estructuras de 4 isómeros de dicha fórmula.
Cuando uno de dichos isómeros se calienta con produce una mezcla de but-2-eno y but-1-eno. Escribe la ecuación química completa indicando de qué tipo de reacción se trata.
Ejercicio 3 · Opción A
3Opción A
2,5 puntosA
Se realiza la electrolisis de una disolución de cloruro de hierro (III) haciendo pasar una corriente de durante por una celda electrolítica.
Describe las reacciones que tienen lugar en el cátodo y en el ánodo de la celda.
Calcula los gramos de hierro depositados.
Calcula el tiempo que tendría que pasar la corriente por la celda para que se desprendan de si dicho volumen se mide a y .
Ejercicio 3 · Opción C
3Opción C
1,5 puntosC
De entre las siguientes estructuras de Lewis del dióxido de azufre ():
1) (con 4 electrones en S)
2)
3)
Selecciona la correcta y justifica por qué las demás son incorrectas.
Describe la geometría de la molécula de empleando el método de repulsión de los pares de electrones de la capa de valencia.
Justifica si la molécula de es polar o no.
Ejercicio 4 · Opción A
4Opción A
2,5 puntosA
Justifica la geometría de las siguientes moléculas covalentes de acuerdo con la teoría de la repulsión de los pares de electrones de la capa de valencia (TRPECV).
Dibromuro de berilio.
Tricloruro de aluminio.
Tetracloruro de silicio.
Explica razonadamente qué tipo de fuerzas hay que vencer para llevar a cabo los siguientes procesos: a) Fundir hielo, b) Hervir bromo (), c) Fundir cloruro de sodio.
Ejercicio 4 · Opción C
4Opción C
1,5 puntosC
Asumiendo que los valores de y de la siguiente reacción no dependen de la temperatura,
Indica si la reacción será espontánea a .
Indica si la reacción será espontánea a .
¿A qué temperatura (en ) pasará de no ser espontánea a ser espontánea?
