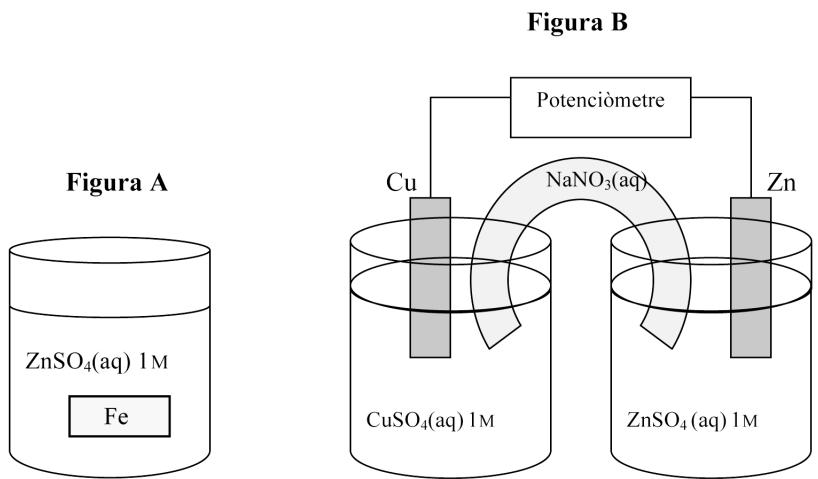
En la experiencia de la figura A, introducimos una pieza de hierro en una solución acuosa de . ¿La pieza de hierro quedará recubierta de una capa de zinc sólido?
QuímicaCataluñaPAU 2012Extraordinaria
Química · Cataluña 2012
7 ejercicios
Ejercicio 1
1
2 puntosCon la ayuda de las figuras, que representan experiencias llevadas a cabo en el laboratorio, conteste las cuestiones siguientes y justifique las respuestas.
Experiencias realizadas en el laboratorio, a
| Par redox | |||
| (V), a |
En la experiencia de la figura B, se conectan las soluciones acuosas de y con un puente salino de . ¿Qué marcará el potenciómetro? ¿Hacia dónde se moverán los iones y ?
Ejercicio 2
2
2 puntosEl hidrógeno es un gas ligero que se usa como combustible para naves espaciales y también, experimentalmente, para autobuses de transporte urbano. Reacciona fácilmente con el oxígeno y produce agua, según la reacción siguiente:
Introducimos en un reactor de hidrógeno y de oxígeno, ambos gases medidos a y a , y a partir de una chispa eléctrica comienza el proceso de combustión para obtener agua líquida.
Calcule el calor liberado si la reacción se produce a presión constante y a .
¿Se liberaría más cantidad de calor si la reacción se produjera a volumen constante y a ? Justifique la respuesta.
Ejercicio 3
3
2 puntosLa lactosa, uno de los principales componentes de la leche, se degrada en contacto con el aire y forma el ácido láctico, . La concentración de este ácido es un parámetro empleado para evaluar la frescura y la calidad de la leche. La acidez media de la leche fresca está normalmente alrededor de de ácido láctico por litro de leche; si la concentración de ácido láctico es superior a por litro, se considera que la leche está cuajada. Para determinar la acidez de una muestra de leche, se valora el ácido láctico de la muestra con una solución acuosa de hidróxido de sodio.
Escriba la reacción de valoración. Explique razonadamente si sería correcto emplear el indicador verde de bromocresol para detectar el punto final de esta valoración.
Valoramos de leche con una solución acuosa de hidróxido de sodio y necesitamos de base para llegar al punto final. Explique razonadamente si la leche está cuajada.
Ejercicio 4
4
2 puntosElija UNA cuestión entre la 4 y la 5.
Un cálculo renal, llamado popularmente piedra en el riñón, es un fragmento de material sólido que se forma dentro del riñón a partir de sustancias que se encuentran en la orina. El cálculo renal más común contiene oxalato de calcio, , una sal que proviene del ácido débil llamado ácido oxálico.
¿Cuál es la solubilidad del oxalato de calcio en agua y a , expresada en , si su producto de solubilidad a la misma temperatura es ?
Disponemos de un poco de oxalato de calcio sólido en contacto con una solución acuosa saturada de esta sal. Explique dos maneras de solubilizar el oxalato de calcio, sin modificar la temperatura.
Ejercicio 5
5
2 puntosElija UNA cuestión entre la 4 y la 5.
El bromuro de metilo se obtiene del metanol mediante una reacción de sustitución catalizada en un medio ácido:
El perfil de la cinética de esta reacción es el siguiente:
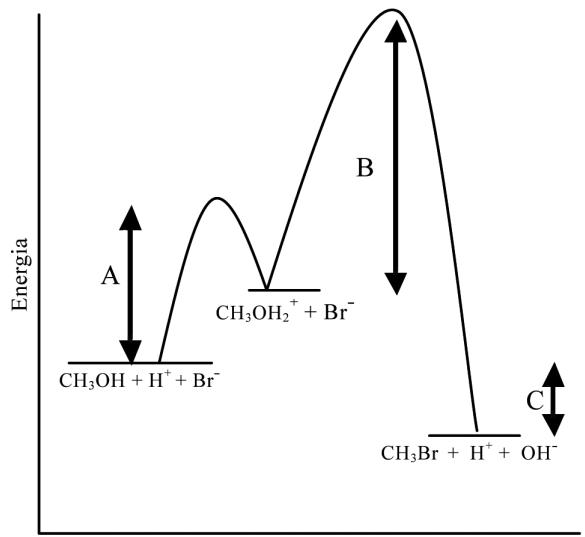
Indique qué magnitudes representan las letras A, B y C. ¿Cuál de las dos etapas del mecanismo de la reacción es la más lenta? ¿La reacción de obtención del bromuro de metilo a partir de metanol en un medio ácido es exotérmica o endotérmica? Justifique las respuestas.
Explique qué se entiende por intermedio de reacción y por estado de transición (o complejo activado). ¿Cuántos intermedios de reacción y cuántos estados de transición hay en el mecanismo de la reacción de obtención del bromuro de metilo a partir de metanol?
Ejercicio 6
6
2 puntosElija UNA cuestión entre la 6 y la 7.
El amoníaco y las soluciones acuosas de este gas desprenden un olor irritante y muy característico que se nota, por ejemplo, en los productos empleados para limpiar cristales. La industria fabrica cada día miles de toneladas de amoníaco mediante la reacción siguiente entre el nitrógeno y el hidrógeno:
Hemos realizado en el laboratorio un experimento en el cual tenemos inicialmente, , los tres compuestos en equilibrio en el reactor. A tiempo hemos introducido nitrógeno al reactor y, mediante un conjunto de sensores que están conectados, hemos obtenido el gráfico siguiente, trabajando siempre a una temperatura determinada:
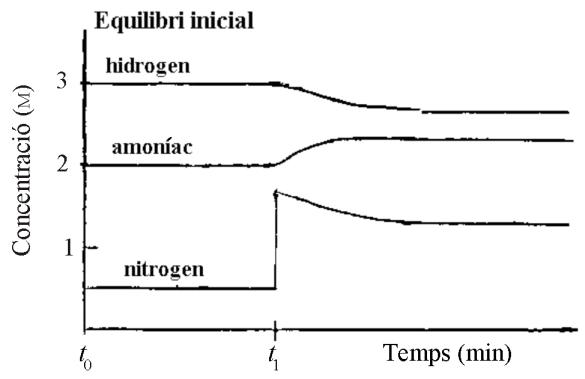
Calcule la constante de equilibrio en concentraciones () de la reacción de obtención de amoníaco, a la temperatura a la que se ha efectuado el estudio.
Explique razonadamente la modificación de la concentración de cada uno de los tres compuestos después de la introducción de nitrógeno al reactor.
Ejercicio 7
7
2 puntosElija UNA cuestión entre la 6 y la 7.
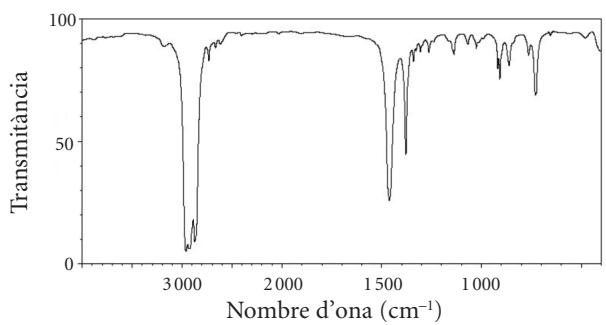
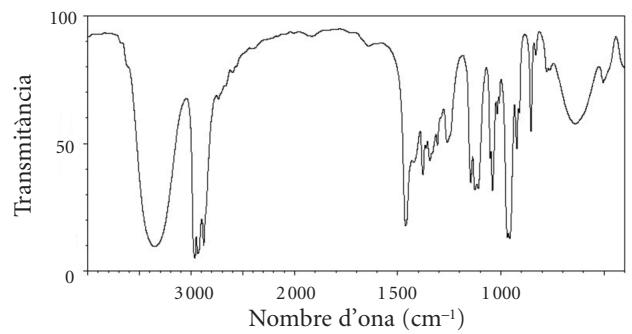
Tenemos dos botellas, A y B, que contienen un líquido puro y transparente que puede corresponder a las sustancias orgánicas siguientes: 3-pentanona , 3-pentanol o pentano . Al no saber qué sustancia hay en cada una de las botellas, hemos sometido las muestras a una espectroscopia infrarroja. Los espectros obtenidos para cada botella son los siguientes:
| Enlace | Número de onda (cm) |
| C-O | 1000-1300 |
| C=O | 1650-1760 |
| C-H | 2850-3000 |
| O-H | 3230-3550 |
Identifique qué sustancia orgánica contiene cada botella. Explique razonadamente la respuesta.
Calcule la temperatura de ebullición del pentano si, en condiciones estándar y a , tiene una entalpía de vaporización de y tiene una entropía de vaporización de . Suponga que las variaciones de entalpía y entropía no se modifican con la temperatura.
