Escriba la configuración electrónica para cada uno de ellos.
QuímicaMurciaPAU 2020Ordinaria
Química · Murcia 2020
10 ejercicios
Ejercicio 1
1
2 puntosDados los elementos Ba (), Tl () y Bi ():
¿Cuál de los tres elementos tendrá un mayor radio atómico? Justifique su respuesta.
¿Alguno de ellos tendrá como número de oxidación principal +1? Justifique su respuesta.
Escriba un posible conjunto de números cuánticos para el electrón diferenciador del Ba.
¿Cuál de los tres elementos es el menos electronegativo? Justifique su respuesta.
Ejercicio 2
2
2 puntosLas siguientes sustancias se encuentran en estado sólido a temperatura ambiente: , y . Explique si en esas condiciones dichas sustancias conducen o no la corriente eléctrica, y por qué.
¿Cuál de las tres sustancias anteriores será más soluble en agua? Justifique su respuesta.
Ordene, justificadamente, según su punto de fusión: , , y .
Ejercicio 3
3
2 puntosUna reacción química transcurre a través las siguientes etapas elementales:
i) lenta
ii) rápida
Escriba la ecuación global para la reacción.
¿Cuál será la ecuación de velocidad de la reacción, el orden de reacción global y las unidades de la constante de velocidad?
Explique si alguna de las especies involucradas en la reacción es un intermedio.
¿Qué le ocurre a la velocidad de reacción () durante el transcurso de la reacción (aumenta, disminuye o permanece constante)? Explique su respuesta.
Ejercicio 4
4
2 puntosEl tetraóxido de dinitrógeno se disocia para dar dióxido de nitrógeno según el siguiente equilibrio:
En una mezcla de los dos gases, a , sus concentraciones son: y .
¿Se encontrará dicha mezcla en equilibrio? Justifique numéricamente su respuesta. En caso de no ser así, ¿cuáles serán las concentraciones de ambos gases cuando se alcance el equilibrio?
¿Cómo afectará al equilibrio un aumento de la presión total del sistema? Justifique su respuesta.
Ejercicio 5
5
2 puntosEl amoniaco es una base débil, cuya constante de basicidad es . Calcule el pH de una disolución de de concentración .
Explique si una disolución de cloruro amónico () en agua será ácida, básica o neutra. No es necesario realizar cálculos numéricos, pero sí explicar los procesos químicos que tienen lugar.
Ejercicio 6
6
2 puntosCalcule el pH de la disolución obtenida al mezclar de con de (considere los volúmenes aditivos).
Calcule el pH de una disolución de .
Ejercicio 7
7
2 puntosDada la siguiente reacción de oxidación-reducción:
Explique cuál es el agente oxidante y cuál el agente reductor.
Ajuste la reacción mediante el método del ion-electrón.
Ejercicio 8
8
2 puntosEn una celda electrolítica se está produciendo la obtención de cobre metálico a partir de fundido, mediante la siguiente reacción:
Escriba las semirreacciones que están teniendo lugar en el ánodo y en el cátodo, indicando si se trata de una oxidación o de una reducción.
Si la intensidad de la corriente eléctrica es de , calcule cuánto cobre metálico se habrá obtenido al cabo de horas.
Explique brevemente la principal diferencia entre una celda electrolítica (como la descrita en este ejercicio) y una celda galvánica (también llamada pila galvánica o voltaica).
Ejercicio 9
9
2 puntosFormule o nombre los siguientes compuestos:
a) ;
b) ;
c) etilenglicol;
d) propil vinil éter;
e) 1-nitropropano
Complete las siguientes reacciones orgánicas con todos los productos mayoritarios esperados, según el tipo de reacción indicado:
Condensación:
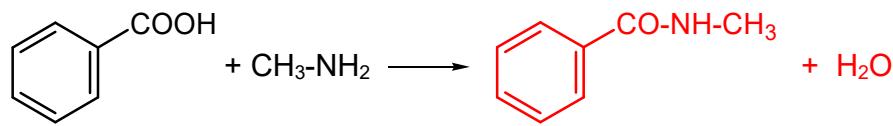
Adición:
Sustitución:
Indique el tipo de reacción orgánica que ha tenido lugar (una sola palabra es suficiente):
a)
b)
Ejercicio 10
10
2 puntosFormule o nombre los siguientes compuestos:
a) Pentan-2-amina
b)
Escriba las fórmulas semidesarrolladas de los siguientes pares de compuestos orgánicos e indique justificadamente el tipo y subtipo de isomería que presentan entre sí:
a) Ácido 3-butenoico y propenoato de metilo
b) Isobutanol y n-butanol
Indique justificadamente el tipo y subtipo de isomería que presentan los siguientes pares de compuestos orgánicos:
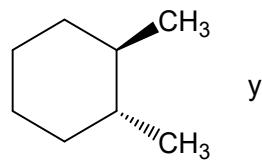
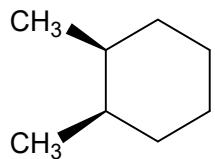
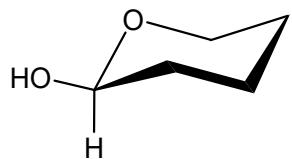
Par de moléculas en conformación de silla (enantiómeros).
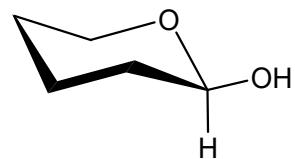
Par de isómeros geométricos de un dimetilciclohexano.