Explique por qué, a temperatura ambiente, el es un gas, el es un líquido y el es un sólido. Razone por qué estos tres elementos forman moléculas diatómicas y es difícil encontrarlos en forma de átomos aislados en la naturaleza. ¿Qué tipo de enlace se establece entre un halógeno y un metal alcalino? Justifique la respuesta y ponga un ejemplo de un compuesto con este tipo de enlace.
QuímicaCataluñaPAU 2025Ordinaria
Química · Cataluña 2025
4 ejercicios90 min de duración
Ejercicio 1
1
2,5 puntosLos halógenos son los elementos que presentan la configuración electrónica de la capa de valencia y se encuentran en la naturaleza formando moléculas diatómicas. El nombre halógeno proviene del griego y significa 'que forma sales'. Por otro lado, los metales alcalinos son los elementos que presentan la configuración electrónica de la capa de valencia .
Los valores de las tablas de abajo corresponden a los radios atómicos y a las energías de ionización de tres elementos: litio, flúor y sodio. Escriba las configuraciones electrónicas de cada elemento. Asigne a cada elemento el radio y la energía de ionización que le corresponden. Razone la respuesta según el modelo atómico de cargas eléctricas. Calcule si un fotón de luz azul de sería capaz de ionizar el átomo que tiene una energía de ionización de .
| Radio atómico (Å) | 1,82 | 0,42 | 2,27 |
| Energía de ionización (kJ mol-1) | 1 681,0 | 496,0 | 520,2 |
Ejercicio 2
2
2,5 puntosEl amoníaco verde no se obtiene a partir de las plantas. Para producirlo hay que conseguir primero hidrógeno verde mediante un proceso de electrólisis del agua con energía eléctrica generada a partir de fuentes renovables. Posteriormente, el hidrógeno reacciona con nitrógeno atmosférico a través de un proceso conocido como síntesis de Haber-Bosch, que permite la obtención de amoníaco en presencia de un catalizador. Este proceso no es económico por las condiciones de presión y temperatura que requiere y el uso de catalizadores. En un reactor de acero de una planta piloto se introduce una mezcla de nitrógeno atmosférico e hidrógeno verde y se calienta a , hasta que se alcanza el equilibrio:
Se analiza el contenido de la mezcla. Los resultados obtenidos se muestran en la tabla siguiente. Escriba la expresión de la constante de equilibrio en concentraciones () de la reacción y calcule su valor a . Calcule también el valor de la constante de equilibrio a .
| Sustancia | Concentración en el equilibrio (mol L-1) |
| 0,142 | |
| 1,84 | |
| 0,36 |
Responda razonadamente a las preguntas siguientes:
— Para obtener un mayor rendimiento de la reacción, ¿es mejor llevar a cabo la reacción a presiones altas o bajas?
— ¿El rendimiento aumenta a temperaturas altas o bajas?
— Según el modelo cinético de colisiones, ¿la reacción se produciría a más velocidad a temperaturas altas o bajas?
Ejercicio 3
3
2,5 puntosEl ácido salicílico o ácido 2-hidroxibenzoico () es un ácido orgánico monoprótico presente en la corteza del sauce. En las farmacias se utiliza para preparar cremas por sus propiedades exfoliantes e hidratantes. Para que la exfoliación sea efectiva la crema debe tener un pH entre y . En una farmacia están haciendo una crema recetada por un dermatólogo en la cual hay gramos de este ácido por cada gramos de crema.
Justifique si esta crema tendrá un pH óptimo para actuar como exfoliante. Indique qué representan los pictogramas del ácido salicílico y de qué peligros nos alertan.


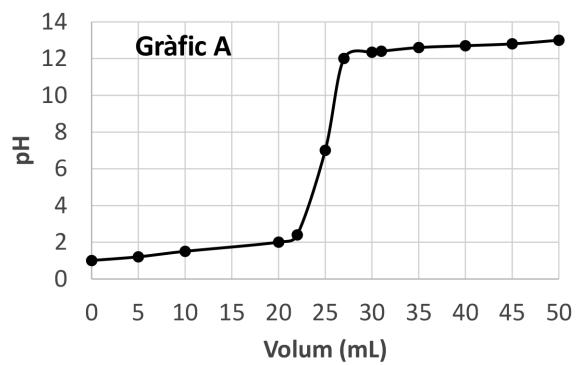
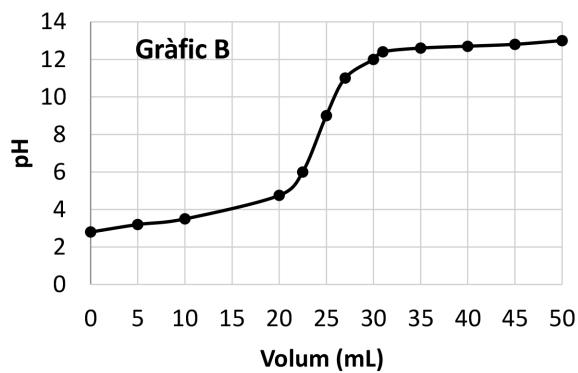
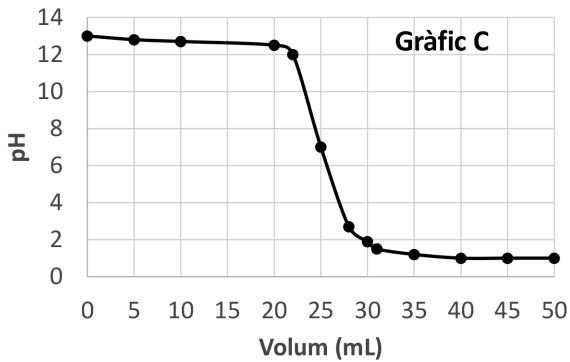
Escriba la reacción de valoración del ácido salicílico con el hidróxido de sodio. Justifique cualitativamente, con las reacciones de hidrólisis necesarias, si el pH en el punto de equivalencia es ácido, básico o neutro. Razone cuál de los tres gráficos siguientes (gráfico A, gráfico B o gráfico C) representa la curva de valoración que se obtiene.
Ejercicio 4
4
2,5 puntosResponda solo a DOS de las cuatro cuestiones planteadas (a, b, c y d).
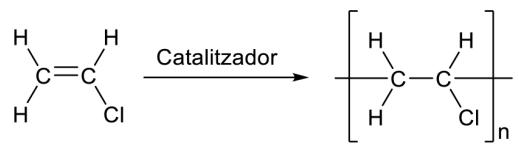
El cloroeteno , también llamado cloruro de vinilo, figura entre los compuestos químicos más producidos en todo el mundo porque es el monómero a partir del cual se obtiene el cloruro de polivinilo (PVC), un plástico bien conocido y muy utilizado para hacer tuberías, persianas o ventanas, entre otras aplicaciones. El cloruro de vinilo se puede obtener a partir de acetileno y cloruro de hidrógeno según la reacción de síntesis siguiente:
Después, este compuesto puede reaccionar fácilmente con el cloro para dar 1,1,2-tricloroetano, un disolvente organoclorado:
| Sustancia | |||
| Entalpía estándar de formación a 298 K (kJ mol-1) | -226,9 | -92,3 | -37,26 |
| Sustancia | C-C | C-H | C=C | Cl-Cl | C-Cl |
| Entalpía de enlace a 25 °C y 1 atmósfera (kJ mol-1) | 348 | 412 | 608 | 242 | 328 |
Explique a partir de qué tipo de reacción de polimerización se obtiene el PVC. Formule todos los isómeros del dicloroeteno y el tricloroetano y diga qué tipo de isomería presentan. Nómbrelos con su nombre sistemático según la IUPAC. Razone si algún isómero del tricloroetano presenta estereoisomería óptica.
Calcule el calor a presión constante y a volumen constante de la reacción de síntesis del cloruro de vinilo en condiciones estándar a . Justifique si esta reacción es endotérmica o exotérmica en estas condiciones.
Calcule la entalpía de la reacción de obtención del 1,1,2-tricloroetano a partir del cloruro de vinilo en condiciones estándar a utilizando las energías de enlace. Razone qué signo tendrá la entropía () de esta reacción y justifique cualitativamente si será espontánea a temperaturas altas o bajas.
Razone qué tipo de reacciones se producen en la obtención del cloruro de vinilo y del 1,1,2-tricloroetano. ¿Qué geometría tiene la molécula de acetileno? Justifique la respuesta según la teoría de repulsión de los pares de electrones de la capa de valencia (RPECV). Razone si la molécula de cloruro de vinilo será polar.
