Para reproducir las condiciones del cilindro de un motor, introducimos de nitrógeno y de oxígeno en un recipiente con una capacidad de y lo calentamos a , que es la temperatura que puede alcanzar la cámara de combustión del motor de un automóvil. Calcule la masa de monóxido de nitrógeno que se formará.
QuímicaCataluñaPAU 2018Extraordinaria
Química · Cataluña 2018
7 ejercicios
Ejercicio 1
1
2 puntosEl monóxido de nitrógeno es un contaminante atmosférico que se origina en el motor de explosión de los automóviles. El aire entra en el cilindro del motor para proporcionar el oxígeno necesario para la combustión de la gasolina, pero como el aire contiene nitrógeno se establece el siguiente equilibrio:
Para mejorar el rendimiento de la combustión de los motores, los fabricantes pueden aumentar la presión o la temperatura de los cilindros. Explique cómo se ve afectada la formación del monóxido de nitrógeno por el aumento de la presión, por un lado, y por el aumento de la temperatura, por el otro.
Ejercicio 2
2
2 puntosEn la industria farmacéutica a menudo es necesario efectuar el análisis de determinados metales. Por ejemplo, para determinar cuantitativamente el hierro que contiene un comprimido multivitamínico, se disuelve este comprimido en ácido y se lleva a cabo la valoración del ion empleando una solución de permanganato de potasio () de concentración conocida. La reacción de valoración es la siguiente:
Justifique que esta reacción de valoración es una reacción redox, y que es espontánea en condiciones estándar y a . Indique, razonadamente, cuál de los reactivos es el oxidante.
En el laboratorio disolvemos un comprimido multivitamínico de masa en un matraz de Erlenmeyer con un poco de ácido. Valoramos esta solución con , y necesitamos para que la solución pase de incolora a lila (punto final de la valoración). Calcule el porcentaje en masa de hierro en el comprimido.
Ejercicio 3
3
2 puntosPara controlar las emisiones de óxidos de nitrógeno () a la atmósfera, las industrias deben modificar los procesos de combustión o llevar a cabo un tratamiento de los efluentes para convertir estos óxidos en sustancias más inocuas. Por ejemplo, el monóxido de nitrógeno se puede reducir a nitrógeno según la reacción química siguiente:
Hemos hecho diversos experimentos para estudiar la cinética de esta reacción a partir de la medición experimental de la velocidad inicial de reacción, y hemos obtenido los resultados siguientes:
| Experimento | Concentración inicial de () | Concentración inicial de () | Velocidad inicial () |
| 1 | 0,60 | 0,37 | |
| 2 | 1,20 | 0,37 | |
| 3 | 1,20 | 0,74 |
Determine el orden de reacción de cada reactivo. Escriba la ecuación de velocidad de la reacción y calcule su constante de velocidad.
Proponemos un mecanismo de reacción para la reducción del monóxido de nitrógeno constituido por las tres etapas elementales siguientes:
Etapa 1:
Etapa 2 (lenta):
Etapa 3:
Explique qué se entiende por intermedio de reacción y por estado de transición (o complejo activado). Diga cuántos intermedios de reacción y cuántos estados de transición hay en el mecanismo de reacción propuesto y justifique las respuestas.
Ejercicio 4
4
2 puntosUn grupo de estudiantes ha montado tres pilas en el laboratorio, y ha medido su fuerza electromotriz, en condiciones estándar y a . Los datos experimentales que han obtenido son los siguientes:
| Pares redox* | |||
| Pila | Polo negativo | Polo positivo | Fuerza electromotriz (V) |
| 1 | +1,62 | ||
| 2 | +1,10 | ||
| 3 | +0,34 | ||
Explique el procedimiento experimental que hay que seguir para construir la pila 2 en el laboratorio y medir su fuerza electromotriz, e indique el material y los reactivos que necesita.
El potencial estándar de electrodo () mide la tendencia de un electrodo a generar un proceso de reducción. Por convenio internacional, al electrodo estándar de hidrógeno a se le asigna un valor de cero y, por tanto, . A partir de las dades experimentales obtenidas, calcule el potencial estándar de reducción del electrodo de , , a una temperatura de .
Ejercicio 5
5
2 puntosLa primera vez que se identificó el helio fue cuando se pudo observar una línea amarilla brillante en el espectro de emisión de un eclipse solar. Posteriormente, se aisló helio en la Tierra tratando un mineral, la cleveíta, y se identificó la emisión de una línea amarilla con una energía de , que se correspondía con la línea observada en el espectro solar.
Calcule la frecuencia y la longitud de onda de un fotón de la línea de emisión identificada para el helio.
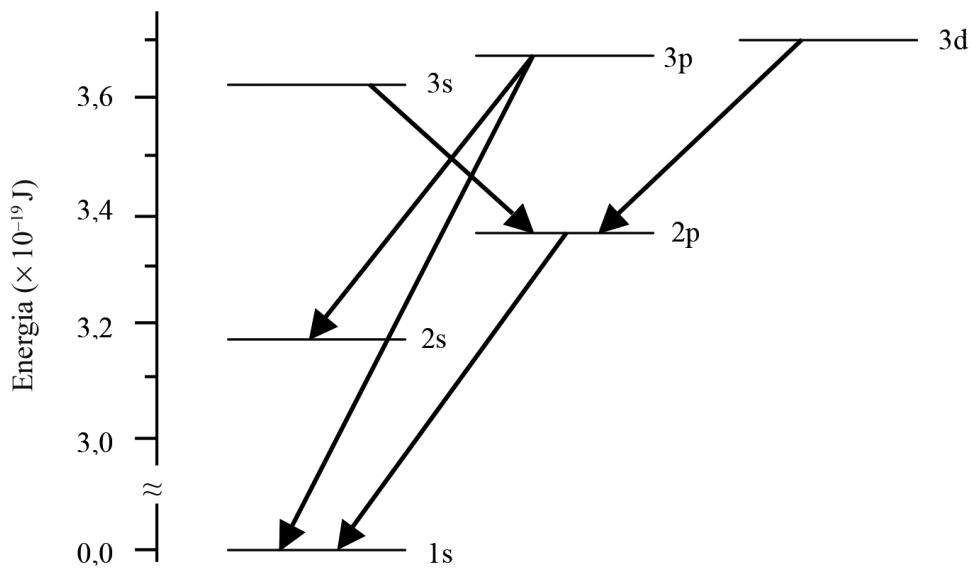
La figura siguiente representa el diagrama de energías de los orbitales atómicos del helio; las flechas indican unas cuantas transiciones electrónicas de emisión permitidas según la espectroscopia. Identifique la transición electrónica correspondiente a la línea amarilla de emisión del helio e indique a qué salto electrónico corresponde. Defina el término orbital atómico según el modelo ondulatorio del átomo y escriba la configuración electrónica del helio antes y después del salto electrónico.
Ejercicio 6
6
2 puntosLa urea () es una sustancia que algunos organismos vivos sintetizan para eliminar el exceso de amoníaco del cuerpo. Observe los datos termodinámicos de la tabla siguiente:
| Reacción | Variación de entalpía a 298 K (kJ) |
| -133,3 | |
| -119,3 | |
| -46,1 | |
| -285,8 | |
| -393,5 |
Calcule la entalpía estándar de formación, a , de la urea sólida.
El proceso de disolución de la urea en agua se puede representar por medio de la ecuación siguiente:
Calcule la variación de entalpía estándar de este proceso de disolución a . Explique de qué manera la temperatura afectará a la disolución de la urea.
Ejercicio 7
7
2 puntosLas Dolomitas, en los Alpes italianos, son unas montañas espectaculares, con rutas de escalada largas y exigentes. Están formadas por roca carbonatada muy dura compuesta principalmente por carbonato de magnesio, a diferencia de las montañas de otros lugares de Europa, en las que predomina el carbonato de calcio.
Escriba la ecuación del equilibrio de solubilidad del carbonato de magnesio y calcule su solubilidad molar en agua a .
Tenemos una muestra de agua, procedente de un charco, que contiene de iones de magnesio y de iones de calcio. Al tomar de esta muestra de agua y añadir de una solución de , observamos que se forma un precipitado blanco. Diga, a partir de los cálculos que considere necesarios, si el precipitado blanco está formado por carbonato de calcio, carbonato de magnesio o una mezcla de ambos, y justifique la respuesta.
