Escriba sus configuraciones electrónicas, identifíquelos e indique a qué grupo y periodo pertenecen.
QuímicaAragónPAU 2024Extraordinaria
Química · Aragón 2024
10 ejercicios
Ejercicio 1
1
2 puntosDados los elementos químicos A, B y C con números atómicos 12, 17 y 30, respectivamente, responda a las siguientes cuestiones de forma razonada:
De los tres elementos, razone cuál tendrá un menor radio atómico y cuál será el más electronegativo.
Justifique qué tipo de enlace (iónico, covalente o metálico) dará lugar a la unión de A-B, B-B y C-C. ¿Cuál será la fórmula del compuesto resultante entre A y B?
Ejercicio 2
2
2 puntosRazone si las siguientes afirmaciones son verdaderas o falsas:
En un átomo, el número máximo de electrones que pueden tener un valor de 3 en su número cuántico principal (n) es 8.
Una disolución acuosa de KI es capaz de conducir la corriente eléctrica.
En la molécula de el nitrógeno tiene dos pares de electrones no compartidos, por lo que la geometría de la molécula es trigonal plana.
La hibridación del átomo de B de la molécula de es .
Ejercicio 3
3
2 puntosObserve el siguiente diagrama de energía potencial para una reacción química, y conteste razonadamente a las preguntas:
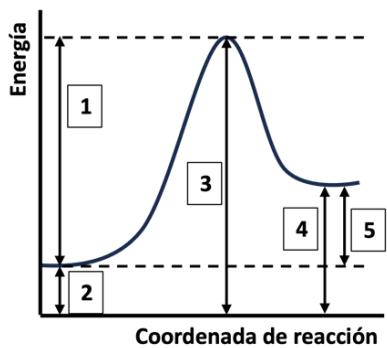
¿Qué intervalo de energía de los mostrados corresponde a la energía de activación de la reacción?
Indique qué intervalos de energía se verán afectados al usar un catalizador. ¿Qué efecto tendrá el catalizador en la velocidad de la reacción?
¿Cuál será el efecto que producirá en la velocidad de la reacción un aumento de la temperatura?
Según este mismo diagrama, ¿qué intervalo de energía nos proporciona la de la reacción? Razone si la reacción es exotérmica o endotérmica.
Ejercicio 4
4
2 puntosSe dispone de una botella de una disolución de (ácido fuerte) que tiene una riqueza en masa del y una densidad de .
Si se toman de la disolución de la botella, ¿hasta qué volumen habrá que diluirlos para que el pH de la disolución sea 2?
¿Cuántos mL de una disolución de habrá que añadir para neutralizar de la disolución obtenida en el apartado anterior? Justifique el pH (ácido, básico o neutro) de la disolución neutralizada.
Ejercicio 5
5
2 puntosConsidere la siguiente reacción química:
Escriba y ajuste la ecuación iónica por el método del ion-electrón y escriba la ecuación molecular completa. Indique el agente oxidante y el reductor.
¿Cuántos gramos de son necesarios para reaccionar con de una disolución de ? ¿Cuál será el rendimiento de la reacción sabiendo que se han obtenido de ?
Ejercicio 6
6
2 puntosUn estudiante construye la pila galvánica que se muestra en la figura en la que uno de los electrodos está formado por una barra de un metal M desconocido sumergido en una disolución de este mismo metal de fórmula . El potencial de la pila resultante es de . En otro experimento adicional, el estudiante sumerge una barra del metal M en una disolución de y observa que empieza a formarse cobre sólido sobre la barra de M. Con la información disponible de los dos experimentos, conteste razonadamente a las siguientes cuestiones:
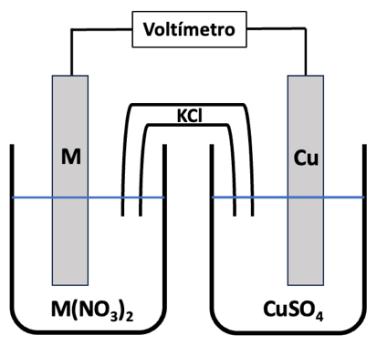
Indique la reacción química que tiene lugar en cada uno de los electrodos de la pila galvánica.
¿Cuál es el valor del potencial estándar de reducción para el metal M? ¿Qué metal es probable que sea M?
¿Qué electrodo de la pila actúa como ánodo y cuál como cátodo? Indique el sentido en el que se moverán los electrones.
Ejercicio 7
7
2 puntosEn la fermentación anaerobia (en ausencia de oxígeno) de una cierta cantidad de glucosa sólida (), a presión de una atmósfera y , se liberan de calor. En dicha fermentación, la glucosa se convierte en etanol () líquido, desprendiéndose además dióxido de carbono.
Escriba y ajuste la ecuación de fermentación de la glucosa y calcule la entalpía molar de la reacción.
¿Cuántos kilos de glucosa se han fermentado para liberar ese calor? Calcule también la masa de etanol que se ha obtenido en esa fermentación.
Si la variación de entropía () de la fermentación de glucosa es , calcule la variación de la energía libre de Gibbs () en las condiciones de fermentación, indicando si el proceso será espontáneo.
Ejercicio 8
8
2 puntosEn un recipiente cerrado se introducen de y de y se calientan hasta . A esa temperatura la reacción que tiene lugar es:
Una vez que se ha alcanzado el equilibrio, la presión parcial del es de y la presión total es de . Calcule:
Los moles de cada sustancia en el equilibrio y el volumen del recipiente.
El valor de las constantes y de para este equilibrio.
Ejercicio 9
9
2 puntosUna forma de producción de ácido nítrico transcurre a través del proceso Ostwald. En la primera etapa de este proceso el amoniaco se oxida a monóxido de nitrógeno:
Para poder obtener una mayor cantidad de NO, ¿podemos aumentar la temperatura? ¿generaríamos más NO al duplicar el volumen del reactor? Conteste razonadamente.
Explique el efecto que tendría en la reacción el ir retirando el a la vez que se va formando.
Razone cómo afectaría al equilibrio la adición de un catalizador.
Ejercicio 10
10
2 puntosLa solubilidad del en agua es de a .
Escriba el equilibrio de solubilidad del hidróxido de cobre y determine el valor de su producto de solubilidad.
¿Cuál será el pH de una disolución saturada de ?
Calcule la solubilidad del (en ) en una disolución de .
