Escriba las reacciones ajustadas correspondientes a los procesos anteriores, así como la correspondiente a la combustión del butano.
QuímicaCastilla-La ManchaPAU 2024Extraordinaria
Química · Castilla-La Mancha 2024
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
3 puntosBloque A
Las entalpías estándar de formación del butano gas , dióxido de carbono gas y del agua líquida son , y , respectivamente.
Calcule la entalpía de combustión del butano en esas condiciones.
Calcule a partir de los datos siguientes la variación de entropía de la reacción, su variación de energía libre y determine si el proceso será espontáneo a la temperatura de .
Ejercicio 2 · Opción A
2Opción A
3 puntosBloque A
Sea la siguiente reacción redox:
Escriba las semirreacciones de oxidación y reducción. Señale claramente cuál es el oxidante y el reductor.
Ajuste las ecuaciones iónica y molecular por el método del ion-electrón.
Calcule los gramos de necesarios para obtener de si el rendimiento de la reacción es del .
Ejercicio 3 · Opción A
3Opción A
3 puntosBloque A
Una disolución acuosa de ácido hipocloroso () tiene un de . Calcule:
La concentración molar de todas las especies presentes en equilibrio.
El grado de disociación del ácido hipocloroso.
El valor de la constante de acidez () del ácido hipocloroso y el valor de la constante de basicidad () de su base conjugada.
Ejercicio 4 · Opción A
4Opción A
3 puntosBloque A
El fosgeno () es un producto gaseoso que se descompone en monóxido de carbono y cloro según el proceso:
En un recipiente de de capacidad se introdujeron de fosgeno, de manera que cuando se alcanzó el equilibrio a la temperatura de , la presión en el interior del matraz fue de . A partir de estos datos, calcule:
El grado de disociación del fosgeno.
La presión parcial de cada componente gaseoso en la mezcla.
El valor de las constantes y .
Ejercicio 5 · Opción B
5Opción B
2 puntosBloque B
Escriba las estructuras de Lewis y describa la geometría de las siguientes moléculas usando la teoría de repulsión de pares de electrones (TRPECV): , , , .
Describa la hibridación de los átomos de de la molécula de eteno () y de la molécula de metano ().
Ejercicio 6 · Opción B
6Opción B
2 puntosBloque B
Explique si el compuesto puede presentar algún tipo de isomería espacial: geométrica, óptica, ambos tipos o ninguno.
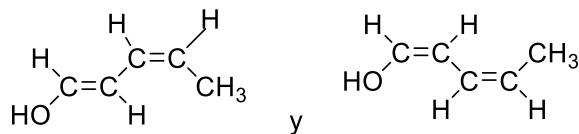
Indique el tipo de isomería que presentan los siguientes pares de compuestos:
Par A:
Par B:
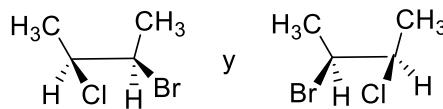
Ejercicio 7 · Opción C
7Opción C
1 puntoBloque C
Conociendo la solubilidad del , calcule su producto de solubilidad.
Ejercicio 8 · Opción C
8Opción C
1 puntoBloque C
Para los siguientes grupos de números cuánticos:
Indique razonadamente cuáles son posibles y cuáles no.
Para las combinaciones correctas, indique el orbital donde se encuentra cada uno de esos electrones y ordénelos en orden creciente de energía.
Ejercicio 9 · Opción C
9Opción C
1 puntoBloque C
Indique si las siguientes afirmaciones son verdaderas o falsas, justificando su respuesta:
Cuanto mayor sea el de una sustancia, mayor será su carácter oxidante.
La reacción de una pila en condiciones estándar transcurre sin necesidad de una fuente de energía externa (proceso espontáneo), generando corriente eléctrica, si .
Ejercicio 10 · Opción C
10Opción C
1 puntoBloque C
Complete en el cuadernillo (NO en este enunciado) las siguientes reacciones orgánicas:
