¿Cuál es la diferencia entre los distintos isótopos de cada elemento? ¿Hay alguna diferencia en sus configuraciones electrónicas?
QuímicaAragónPAU 2016Ordinaria
Química · Aragón 2016
10 ejercicios90 min de duración
Ejercicio 1 · Opción A
1Opción A
1,5 puntosCromo y cloro son elementos que se encuentra en la naturaleza como mezcla de isótopos estables: , y para cromo; y para cloro. Responda de forma justificada a las siguientes cuestiones:
Escriba la configuración electrónica del isótopo más abundante de cada elemento: y .
Escriba los números cuánticos posibles para los electrones más externos del cloro.
Ejercicio 1 · Opción B
1Opción B
2 puntosResponda razonadamente a las siguientes cuestiones:
¿Qué geometría presentan las moléculas , y de acuerdo con el modelo de repulsión de pares electrónicos? ¿Por qué tiene el punto de ebullición más alto y es la más polar de las tres?

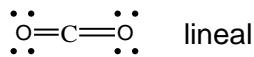
¿Qué tipo de hidrocarburos son los reactivos y productos de las siguientes ecuaciones? y ¿cuál es el cambio de hibridación en los átomos de carbono al producirse las reacciones?
Ejercicio 2 · Opción A
2Opción A
1,5 puntosResponda a las siguientes preguntas:
¿Cuál de las siguientes especies será capaz de oxidar : o ? Escriba las ecuaciones de oxidación y reducción ajustadas por el método del ión-electrón.
¿Cuál será el resultado de la electrólisis de acuoso?
Ejercicio 2 · Opción B
2Opción B
1,5 puntosLa reacción: es de primer orden respecto a oxígeno y de segundo respecto a monóxido de carbono.
Escriba la ecuación de velocidad y las unidades de la constante de velocidad. Calcule el orden total de la reacción.
¿Qué sucederá con la velocidad si aumenta la temperatura de la reacción?
¿Afectará a la velocidad la disminución del volumen a temperatura constante?
Ejercicio 3 · Opción A
3Opción A
2 puntosRazone con los correspondientes equilibrios en disolución acuosa si las siguientes especies tienen carácter ácido, básico o anfótero: ion hidrogenocarbonato, ion carbonato, ion hidrogenosulfuro y amoníaco.
Determine si reaccionará con las siguientes sustancias: , y . Escriba las correspondientes reacciones ajustadas.
Justifique qué hidróxido presentará mayor solubilidad en disolución acuosa: o .
Ejercicio 3 · Opción B
3Opción B
1,5 puntosJustifique la veracidad o falsedad de las siguientes afirmaciones:
Para un equilibrio, nunca puede ser más pequeña que .
Para aumentar la concentración de en el equilibrio: ; , tendremos que calentar el sistema.
Un aumento de presión en el siguiente equilibrio: aumenta la producción de metano gaseoso.
Ejercicio 4 · Opción A
4Opción A
2,5 puntosEn la combustión de de una mezcla de moles de butano y moles de propano a y de presión se liberan . Calcule:
El número total de moles .
Las entalpías de combustión de butano y propano. Escriba sus ecuaciones.
Los moles de butano y los de propano.
Ejercicio 4 · Opción B
4Opción B
2,5 puntosEl permanganato de potasio reacciona con agua oxigenada (peróxido de hidrógeno) en disolución de ácido sulfúrico dando lugar a oxígeno, sulfato de manganeso (II), sulfato de potasio y agua.
Escriba la ecuación correspondiente, ajústela por el método del ion-electrón e indique cuál es el oxidante y cuál el reductor.
Si se consumen de una disolución de permanganato potásico para valorar de agua oxigenada, ¿cuál será la concentración del agua oxigenada?
Calcule el volumen de oxígeno molecular desprendido en la valoración del apartado b, medido a y .
Ejercicio 5 · Opción A
5Opción A
2,5 puntosSe introduce fosgeno en un recipiente vacío de de volumen a una presión de y una temperatura de , produciéndose su descomposición según el equilibrio: Sabiendo que en estas condiciones el valor de vale ; calcule:
La concentración inicial de fosgeno.
Las concentraciones de todas las especies en el equilibrio.
La presión parcial de cada uno de los componentes en el equilibrio.
Ejercicio 5 · Opción B
5Opción B
2,5 puntosSe prepara una disolución de ácido benzoico disolviendo del ácido en agua para obtener de disolución. Sabiendo que el ácido disocia en un :
Calcule la constante de disociación del ácido y el pH de dicha disolución.
Si sobre la disolución anterior adicionamos de (sin cambio de volumen) dando lugar a una disolución reguladora, ¿cuál será el pH de la disolución resultante?
