Defina el término primera energía de ionización de un elemento e indique qué signo tiene. Escriba la configuración electrónica del sodio antes y después del proceso de ionización. Defina el término segunda energía de ionización e indique qué signo tiene. Explique razonadamente, basándose en las configuraciones electrónicas y el modelo atómico de cargas eléctricas:
— si el radio del sodio será mayor o menor que el del ion sodio;
— si la segunda energía de ionización del sodio será mayor o menor que la primera energía de ionización.
QuímicaCataluñaPAU 2023Extraordinaria
Química · Cataluña 2023
7 ejercicios90 min de duración
Ejercicio 1
1
2,5 puntosEn el alumbrado público se utilizan diferentes lámparas de descarga que contienen un gas, como las de vapor de sodio a alta presión. La luz se consigue por excitación del gas mediante la energía suministrada por una descarga eléctrica entre dos electrodos. Las lámparas de vapor de sodio tienen una vida limitada, ya que si la descarga eléctrica es muy grande, puede producir la ionización del sodio.
Si la energía de ionización del estado fundamental del sodio es , calcule la longitud de onda de la radiación capaz de ionizar el sodio gaseoso. Calcule también la energía necesaria para ionizar de sodio gaseoso desde su estado fundamental.
Ejercicio 2
2
2,5 puntosEl cloroetano (), también llamado cloruro de etilo, se ha utilizado a lo largo de la historia como anestésico de uso tópico y de acción rápida que actúa por enfriamiento local en el área aplicada. Actualmente se recomienda evitar el contacto físico con esta sustancia. Para obtener cloroetano, se pueden utilizar dos métodos diferentes que se basan en las reacciones siguientes:
1ª reacción:
2ª reacción:
| Sustancia | |||
| -104,9 | -92,3 | -84,7 |
Si los valores de las entropías estándar a son y para la primera y para la segunda reacción respectivamente, compruebe que las dos reacciones son espontáneas a la temperatura de . Justifique la respuesta. Explique qué indica, a escala microscópica, el signo de la variación de entropía estándar de estas dos reacciones.
Las fichas de seguridad del cloroetano (pictogramas 1 y 2) y del ácido clorhídrico (pictogramas 3 y 4) contienen los símbolos siguientes:
¿Qué quieren decir estos pictogramas de seguridad y de qué peligros nos advierten?



Ejercicio 3
3
2,5 puntosEl dióxido de azufre es un gas que se origina sobre todo durante la combustión de combustibles fósiles que contienen azufre (petróleo y combustibles sólidos como el carbón), aunque también se puede producir a partir del trióxido de azufre () según la reacción siguiente:
| T (K) | 298 | 400 | 600 | 800 | 1 000 |
En la tabla adjunta se recogen los valores, a diferentes temperaturas, de la constante de equilibrio en concentraciones () de esta reacción. Razone cómo afecta al equilibrio y a la un incremento de temperatura, tanto si la reacción es endotérmica como si es exotérmica. Justifique si la reacción de formación de dióxido de azufre es exotérmica o endotérmica. Explique cómo afecta al equilibrio y al rendimiento de la reacción:
— un aumento de la presión, manteniendo la temperatura constante;
— un aumento del volumen, manteniendo la temperatura constante.
Colocamos una cantidad de trióxido de azufre en un recipiente cerrado de a . Comprobamos que en el equilibrio hay de oxígeno. Calcule las concentraciones de las sustancias presentes en el equilibrio.
Ejercicio 4
4
2,5 puntosEn la figura adjunta se muestran dos gráficas (A y B) correspondientes a dos curvas de valoración de dos ácidos diferentes con hidróxido de sodio (). Una curva corresponde a la valoración de ácido clorhídrico y la otra curva a la valoración de ácido acético (), un ácido carboxílico monoprótico débil, llamado también ácido etanoico. Considere que en ambos casos se ha valorado el mismo volumen de ácido de la misma concentración.
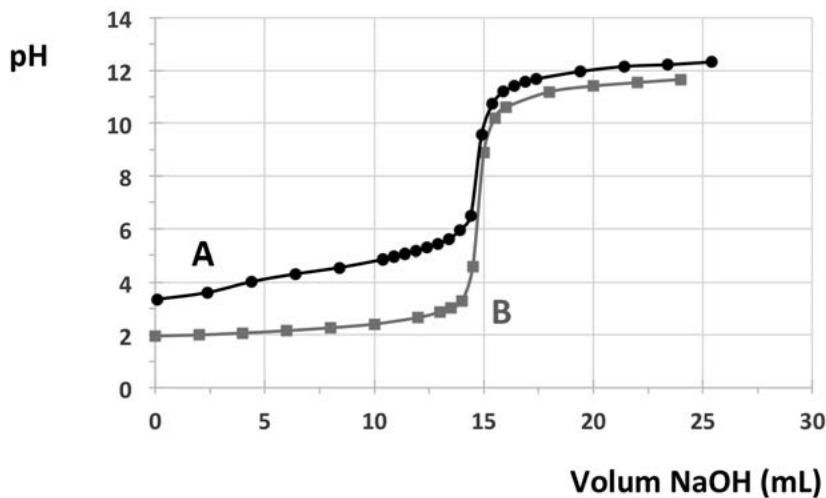
Escriba las dos reacciones de valoración. Justifique qué curva de valoración corresponde a cada ácido según el pH en el punto de equivalencia.
Si para valorar de una solución de ácido acético se gastan de hidróxido de sodio , ¿cuál es la concentración del ácido acético? Razone si es una buena elección utilizar anaranjado de metilo como indicador en esta valoración.
| Indicador | Intervalo pH | Cambio de color | |
| Ácido | Alcalino | ||
| Anaranjado de metilo | 3,1-4,4 | rojo | amarillo |
| Verde de bromocresol | 3,8-5,4 | amarillo | verde azulado |
| Azul de bromotimol | 6,0-7,6 | amarillo | azul |
| Fenolftaleína | 8,0-9,5 | incoloro | fucsia |
| Nitramina | 11,0-13,0 | incoloro | marrón anaranjado |
Ejercicio 5
5
2,5 puntosEl dióxido de nitrógeno es un gas contaminante que se forma como subproducto en los procesos de combustión a altas temperaturas, como en los vehículos motorizados y las plantas eléctricas. Por eso es un contaminante frecuente en las zonas urbanas. El dióxido de nitrógeno se puede obtener también por la oxidación del monóxido de dinitrógeno según la reacción:
| Sustancia | ||
| Entalpía estándar de formación a 298 K () | 81,6 | 33,2 |
| Sustancia | |||
| Entropía molar estándar absoluta a 298 K () | 220,1 | 240,1 | 205,2 |
Calcule la entalpía, la variación de entropía y la variación de energía de Gibbs de la reacción. Indique si se trata de un proceso espontáneo en estas condiciones, y en qué intervalo de temperaturas lo será. Suponga que la entalpía y la entropía no varían con la temperatura.
Haga una representación gráfica aproximada que muestre la energía en función de la coordenada de reacción. Suponga que la reacción de oxidación del monóxido de dinitrógeno es una reacción lenta y que su mecanismo solo tiene una etapa, y señale en ella la energía de activación, el estado de transición y la variación de entalpía de la reacción. Si añadimos un catalizador para acelerar la reacción, ¿modificaremos el valor de la energía de activación? ¿Y el valor de la entalpía de la reacción? Justifique las respuestas.
Ejercicio 6
6
2,5 puntosLa descarbonización del planeta es uno de los grandes retos mundiales para combatir el cambio climático. Para conseguirlo, se postula el hidrógeno como la principal alternativa a los combustibles fósiles. Ahora bien, para alcanzar una descarbonización completa hay que producir el hidrógeno de una manera sostenible. El llamado hidrógeno verde se obtiene por electrólisis del agua, esto es, la descomposición del agua en hidrógeno y oxígeno aplicando una corriente eléctrica, pero utilizando electricidad obtenida de fuentes renovables.
Indique las semirreacciones que tienen lugar en el cátodo y el ánodo en un proceso de electrólisis del agua. Indique la reacción global. Razone, cualitativamente, en cuál de los dos electrodos se liberará más gas a de presión y a .
Se prepara una celda electrolítica con una solución que contiene ácido sulfúrico () y se hace pasar durante una corriente eléctrica de . Calcule el volumen de hidrógeno producido, medido a de presión y a . Considere la solución suficientemente ácida y que el hidrógeno se comporta idealmente.
Ejercicio 7
7
2,5 puntosEl yoduro de plomo(II) () es una sal poco soluble de un color amarillo muy intenso. Antiguamente, el yoduro de plomo(II) era utilizado por los artistas como pigmento, con el nombre de amarillo de yodo, pero debido a su toxicidad y baja estabilidad dejó de utilizarse.
Escriba el equilibrio de solubilidad del yoduro de plomo(II) y calcule su solubilidad molar a . Explique razonadamente si la solubilidad del yoduro de plomo(II) en agua es mayor o menor que su solubilidad en una solución de yoduro de sodio ().
Calcule la concentración de ion plomo(II) necesaria para que precipite yoduro de plomo(II) a partir de una solución de yoduro de potasio () de concentración . Si tenemos dos soluciones de la misma concentración, una de yoduro de potasio y la otra de cloruro de potasio (), ¿cuál de las dos necesitará una concentración más alta de para empezar a precipitar, en el primer caso y en el segundo ? Justifique la respuesta.
