Escriba y ajuste la ecuación iónica por el método del ion-electrón y escriba la ecuación molecular completa. Indique el agente oxidante y el reductor.
QuímicaAragónPAU 2024Ordinaria
Química · Aragón 2024
10 ejercicios
Ejercicio 1
1
2 puntosCuando reacciona aluminio con clorato de potasio en presencia de ácido clorhídrico se obtiene cloruro de aluminio, cloruro de potasio y agua.
Si partimos de de aluminio y de una disolución de clorato de potasio, calcule los gramos de cloruro de aluminio que se obtendrían.
Ejercicio 2
2
2 puntosResponda razonadamente a las siguientes cuestiones:
Considere la siguiente reacción sin ajustar y los potenciales estándar de reducción de los reactivos:
;
¿En qué sentido, derecha o izquierda, transcurrirá esta reacción de forma espontánea? ¿Qué reactivo es el que se reduce y cuál se oxida en la reacción espontánea?
En la reacción de potasio con azufre: , ¿son verdaderas o falsas las siguientes afirmaciones? Indique la semirreacción que ocurre en cada caso:
El potasio capta electrones y por lo tanto es el oxidante.
El azufre es la especie que se reduce.
Ejercicio 3
3
2 puntosLa solubilidad en agua del , a , es de .
Escriba el equilibrio de solubilidad del , calcule el valor de su producto de solubilidad y las concentraciones molares de los iones fluoruro y magnesio en una disolución saturada.
Se disuelven de en de agua, ¿cuál será la cantidad máxima de , en gramos, que podemos añadir a esa disolución sin que precipite ? Considere que el está totalmente disociado y que el volumen no cambia al añadir el .
Ejercicio 4
4
2 puntosLa velocidad de la reacción se ha estudiado a de temperatura. Los experimentos realizados se muestran en la siguiente tabla:
| Experimento | (mol·L) | (mol·L) | (mol·L·s) |
| 1 | 0,25 | 0,25 | 0,015 |
| 2 | 0,25 | 0,50 | 0,030 |
| 3 | 0,50 | 0,50 | 0,120 |
Deduzca los órdenes parciales de los reactivos y el orden total de la reacción. Escriba también la expresión de la ecuación de velocidad.
Calcule la constante de velocidad, , y especifique sus unidades.
Indique, de forma razonada, si sería posible aumentar la velocidad de reacción en el experimento 1 sin modificar la concentración de los reactivos ni aumentar la temperatura.
Ejercicio 5
5
2 puntosConsidere los elementos químicos X e Y con números atómicos 56 y 16, respectivamente, y razone si son verdaderas o falsas las siguientes cuestiones:
Los números cuánticos del último electrón (electrón diferenciador) del elemento con número atómico 56 son .
La combinación de los dos elementos dará un compuesto de fórmula XY.
El elemento X es el más electronegativo de los dos, pero Y tiene un mayor radio atómico.
El catión es isoelectrónico con el ion más probable del elemento Y.
Ejercicio 6
6
2 puntosLas estructuras de Lewis de las moléculas y son las que se muestran en la figura de la derecha.
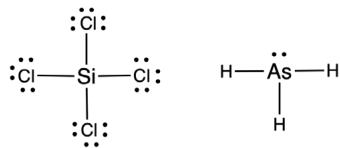
Prediga sus geometrías moleculares según la teoría de repulsión de pares de electrones de la capa de valencia (TRPECV). Razone si sus geometrías electrónicas coinciden con las moleculares.
Deduzca la hibridación del átomo central de la molécula de . Razone la respuesta.
Explique si alguna de estas moléculas puede formar enlaces de hidrógeno.
Ejercicio 7
7
2 puntosUna de las etapas de la fabricación industrial de ácido nítrico consiste en la siguiente reacción entre dióxido de nitrógeno y agua:
Calcule la entalpía de la reacción anterior a partir de los siguientes datos e indique si es una reacción endotérmica o exotérmica:
A:
B:
C:
¿Cuánto calor se pondrá en juego si se quieren obtener de ácido nítrico? ¿Qué volumen de , medido a y , se obtendrá junto a ese ácido nítrico?
Ejercicio 8
8
2 puntosConsidere las siguientes reacciones:
A)
B) ¿?
Indique las expresiones de de ambos procesos. Teniendo en cuenta el valor de para la reacción A, calcule el valor de para la reacción B.
Justifique si son verdaderas o falsas las siguientes afirmaciones sobre este proceso:
El valor de es igual al valor de .
Un aumento de la temperatura de reacción mejorará la producción de metano.
Ejercicio 9
9
2 puntosSe prepara una disolución acuosa de una base () cuyo pH es . Plantee el equilibrio ácido-base y calcule la de dicha base y su grado de disociación.
Se quiere neutralizar con el presente en de una disolución de comercial que tiene una riqueza en masa del y una densidad de . Disponemos de de ¿serán suficientes para llevar a cabo esa neutralización?
Ejercicio 10
10
2 puntosConsidere la siguiente tabla de especies ácidas y básicas:
| Ácido | Base | ||
Complete las casillas en blanco de la tabla incorporando la fórmula del ácido o de la base conjugada y o , según corresponda. Justifique las respuestas.
Ordene los ácidos recogidos en la tabla de mayor a menor fortaleza. Razone la respuesta.
Se neutraliza completamente una disolución de con otra de . Justifique el pH (ácido, básico o neutro) de la disolución neutralizada.
