Escriba la configuración electrónica del Po ().
QuímicaMurciaPAU 2021Extraordinaria
Química · Murcia 2021
10 ejercicios90 min de duración
Ejercicio 1
1
2 puntosExplique si el conjunto de números cuánticos es posible o no para un electrón en un átomo. En caso de ser posible, indique en qué nivel de energía (capa) y tipo de orbital (subcapa) se encontraría el electrón.
Dados los elementos: (), (), (), (), (), (), () y (), explique brevemente cuál de ellos: a) tiene un mayor radio atómico; b) tiene tendencia a ganar dos electrones; c) es el más electronegativo; d) presenta una reactividad química muy baja. (No se repiten las respuestas).
Ejercicio 2
2
2 puntosRepresente la estructura de Lewis de la fosfina, , y en base a ella explique la geometría y polaridad de dicha molécula.
Explique por qué el punto de ebullición del () es mucho mayor que el de la fosfina, ().
Las siguientes sustancias son sólidas a temperatura ambiente: , , y . ¿Cuál de ellas es un sólido dúctil y maleable? Justifique su respuesta.
Ejercicio 3
3
2 puntosLa descomposición de a transcurre a través del siguiente mecanismo, en dos etapas elementales:
i) lenta
ii) rápida
Escriba la ecuación global para la reacción.
¿Cuál será la ecuación de velocidad de la reacción, el orden de reacción global y las unidades de la constante de velocidad?
Explique si alguna de las especies involucradas en la reacción es un intermedio.
¿Cómo afectará a la velocidad de reacción y a la constante de velocidad un aumento de ?
Ejercicio 4
4
2 puntosSabiendo que a la solubilidad del en agua es , calcule la constante del producto de solubilidad () de dicha sal.
¿Qué cantidad, en moles, de iones habrá presentes en de una disolución saturada de a ?
Si la disolución saturada de está en equilibrio con de , razone cualitativamente qué ocurrirá con la cantidad de iones en disolución si:
Se retira de .
Se aumenta la . (La disolución de en agua es un proceso endotérmico).
Se retiran aniones de la disolución (por ejemplo, precipitándolos como ).
Ejercicio 5
5
2 puntosCalcule el pH de una disolución de de a la que se adicionan de , suponiendo que el volumen de la disolución no varía.
Datos
- Masas atómicas:
Explique si una disolución de en agua será ácida, básica o neutra. No es necesario realizar cálculos numéricos, pero sí explicar los procesos químicos que tienen lugar.
Ejercicio 6
6
2 puntosUna disolución acuosa de ácido cianhídrico () presenta un . Calcule:
La concentración, , de dicha disolución.
El grado de disociación del .
Datos
Explique si una disolución de en agua será ácida, básica o neutra. No es necesario realizar cálculos numéricos, pero sí explicar los procesos químicos que tienen lugar.
Ejercicio 7
7
2 puntosDada la siguiente reacción de oxidación-reducción:
Explique cuál es el agente oxidante y cuál el reductor. ¿Cuál de ellos capta electrones?
Ajuste la reacción mediante el método del ion-electrón.
Ejercicio 8
8
2 puntosTeniendo en cuenta los siguientes potenciales estándar de reducción:
Explique cuál de los tres metales (, o ) es más oxidante.
Justifique numéricamente si será posible reducir iones , en condiciones estándar, adicionando virutas de o de . Escriba y ajuste las hipotéticas reacciones que tendrían lugar.
Indique en qué electrodo (cátodo o ánodo) tienen lugar las reacciones de oxidación y reducción en una pila o celda galvánica, y hacia qué electrodo circulan los electrones.
Escriba la expresión general para la fuerza electromotriz de una pila (). ¿Cómo tiene que ser su signo para que la pila funcione?
Ejercicio 9
9
2 puntosFormule o nombre los siguientes compuestos:
a) propen-2-ol; b) ácido oxálico; c) ; d) ; e)
Complete las siguientes reacciones orgánicas con todos los productos mayoritarios esperados:
a) Adición:
b) Sustitución:
c) Eliminación:
Indique el tipo de reacción orgánica que ha tenido lugar (una sola palabra es suficiente):
a)
b)
Ejercicio 10
10
2 puntosFormule o nombre los siguientes compuestos: a) Ácido 2-etilbutanoico; b)
Escriba las fórmulas semidesarrolladas los siguientes pares de compuestos orgánicos e indique el tipo y subtipo de isomería que presentan entre sí:
a) etilciclohexano y 1-etil-3-metilciclopentano
b) n-propanol e isopropanol
Explique si el compuesto puede presentar algún tipo de isomería espacial (geométrica, óptica, ambos tipos o ninguno).
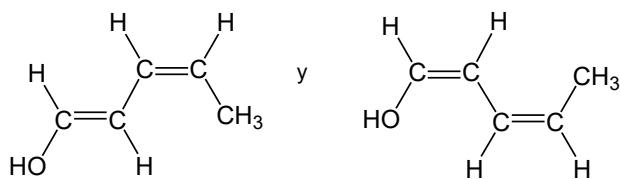
Indique el tipo y subtipo de isomería que presenta el siguiente par de compuestos: