Escriba las reacciones de valoración de los dos ácidos. Indique razonadamente si el pH en el punto de equivalencia de cada una de las dos valoraciones es ácido, neutro o básico.
QuímicaCataluñaPAU 2018Ordinaria
Química · Cataluña 2018
7 ejercicios
Ejercicio 1
1
2 puntosLa figura muestra las curvas obtenidas en la valoración del ácido acético —llamado también ácido etanoico— (curva A) y del ácido clorhídrico (curva B) con hidróxido de sodio ().
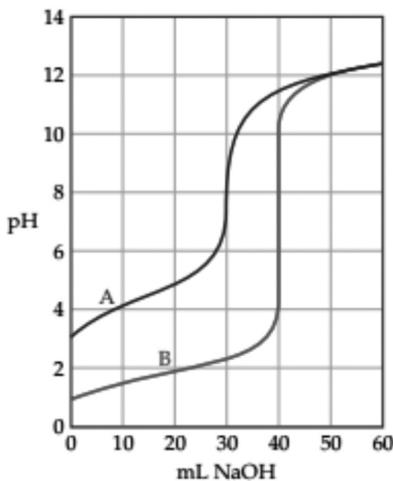
Indique el material y los reactivos que utilizaría en el laboratorio para valorar mL de una solución de ácido clorhídrico de concentración desconocida con una solución de hidróxido de sodio M. Explique el procedimiento experimental que seguiría.
Ejercicio 2
2
2 puntosLas lámparas de descarga contienen un gas, como por ejemplo , que se excita mediante la energía suministrada por una descarga eléctrica. Posteriormente, cuando el gas vuelve a su estado fundamental, se produce la emisión de luz.
Las farolas de vapor de sodio, utilizadas habitualmente para la iluminación pública porque son muy eficientes, son un tipo de lámparas de descarga que emiten una luz amarilla brillante con una longitud de onda de nm.
Calcule la frecuencia y la energía de esta radiación electromagnética.
Las farolas de vapor de sodio tienen una vida limitada, ya que, en determinados momentos, la descarga eléctrica suministrada a la farola puede producir una energía muy alta y superior a la primera energía de ionización del sodio. Defina el término primera energía de ionización de un elemento y escriba la configuración electrónica del sodio antes y después de esta descarga de alta energía. Explique razonadamente, a partir del modelo atómico de cargas eléctricas, si la segunda energía de ionización del sodio será mayor o menor que la primera energía de ionización.
Ejercicio 3
3
2 puntosEn un instituto, utilizan un hornillo de alcohol para calentar los de agua que contiene un vaso de precipitados, en condiciones estándar y a una temperatura de . Cuando el tipo de alcohol que quema en el hornillo es etanol, se produce la reacción de combustión siguiente:
| Enlace | C-C | C-O | C-H | O-H | C=O |
| Entalpía de enlace (kJ mol-1) en condiciones estándar y a 298 K | 348 | 360 | 412 | 463 | 797 |
Calcule el calor desprendido cuando se han consumido de etanol y determine la temperatura final que alcanzará el agua. Considere que el calor absorbido por el ambiente y por el vaso de precipitados es despreciable.
Calcule la entalpía del enlace .
Ejercicio 4
4
2 puntosElija UNA cuestión de entre la 4 y la 5.
El cobalto es un metal indispensable para mejorar el rendimiento de los automóviles eléctricos, y también se utiliza para que las baterías de los teléfonos móviles duren más tiempo. Mediante la electrólisis de una solución de yoduro de cobalto(II) () podemos obtener cobalto metálico y yodo ().
Haga un dibujo esquemático de este proceso electrolítico, e indique el nombre y la polaridad de los electrodos. Escriba la semirreacción que tiene lugar en el electrodo de polaridad positiva.
Calcule la masa de cobalto que obtendremos en uno de los electrodos cuando hagamos pasar una corriente de a través de una solución de yoduro de cobalto(II) durante minutos.
Ejercicio 5
5
2 puntosElija UNA cuestión de entre la 4 y la 5.
El fosgeno () es una sustancia empleada en la fabricación de polímeros como los policarbonatos o los poliuretanos. Este compuesto se puede disociar según la ecuación siguiente:
Introducimos una cantidad determinada de fosgeno en un recipiente y lo calentamos hasta que llega a . Una vez se ha alcanzado el equilibrio, la presión total en el recipiente es de y la presión parcial del monóxido de carbono, igual que la del cloro, es de .
Calcule la constante de equilibrio en presiones de la reacción de disociación del fosgeno a . Indique si la constante de equilibrio en concentraciones y la constante de equilibrio en presiones de esta reacción tienen el mismo valor a y justifique la respuesta.
Manteniendo siempre la temperatura a , ¿cómo se puede ver afectada la disociación del fosgeno si, cuando se ha llegado al equilibrio, provocamos una disminución del volumen del recipiente? ¿Y si añadimos un catalizador? ¿Se modificará en alguno de los dos casos la constante de equilibrio en presiones? Justifique las respuestas.
Ejercicio 6
6
2 puntosElija UNA cuestión de entre la 6 y la 7.
La azurita es un mineral que contiene, entre otras sustancias, hidróxido de cobre(II). Se utiliza bastante en joyería porque es de un color azul intenso muy característico.
¿Qué masa de hidróxido de cobre(II) podemos disolver si una pieza de joyería que contiene azurita cae en un recipiente en el que hay de agua acidulada con un pH de ? Exprese el resultado en miligramos.
¿La solubilidad del hidróxido de cobre(II) en agua destilada es más alta o más baja que en una solución acuosa de ? ¿La formación de complejos de cobre(II), añadiendo por ejemplo , aumenta o disminuye la solubilidad del hidróxido de cobre(II)? Justifique las respuestas.
Ejercicio 7
7
2 puntosElija UNA cuestión de entre la 6 y la 7.
La actividad antimicrobiana de la plata ha sido demostrada in vitro incluso contra bacterias multirresistentes. Para que se dé esta actividad, es necesario que la plata se encuentre en el estado de oxidación +1, como sucede en el óxido de plata. Pero a una temperatura de , este compuesto se puede descomponer y puede formar plata en el estado de oxidación 0, según la reacción química siguiente:
En el gráfico siguiente se muestra la variación de la energía libre estándar de esta reacción en función de la temperatura:
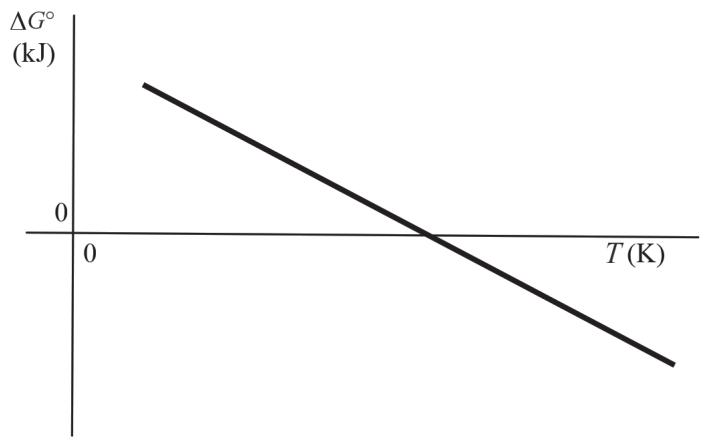
Calcule la variación de entropía estándar () de la reacción de descomposición del óxido de plata a . Explique qué indica, a escala microscópica, el signo de la variación de esta magnitud termodinámica.
Explique cuál es la influencia de la temperatura en la espontaneidad de esta reacción. Diga si la reacción es exotérmica o endotérmica y justifique la respuesta.
