A temperatura ambiente es líquido y es sólido.
QuímicaMurciaPAU 2017Extraordinaria
Química · Murcia 2017
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2,2 puntosIndique razonadamente la veracidad o falsedad de las siguientes afirmaciones:
La sustancia conduce la corriente eléctrica en estado sólido.
La molécula de es apolar porque sus enlaces C-Cl presentan momento dipolar nulo.
Ejercicio 1 · Opción B
1Opción B
2,2 puntosJustifique la veracidad o falsedad de las siguientes afirmaciones.
El número de oxidación más probable para el elemento de es .
es un conjunto posible de valores para los números cuánticos del electrón más externo del átomo de .
Para el elemento de , su primera energía de ionización es menor que su segunda energía de ionización.
y tienen el mismo número de protones.
Ejercicio 2 · Opción A
2Opción A
2 puntosSea una disolución acuosa de de concentración . Calcule:
La constante de basicidad del .
El grado de disociación del .
Ejercicio 2 · Opción B
2Opción B
2 puntosSabiendo que el producto de solubilidad () de la especie es igual a :
Calcule el pH de una disolución saturada de dicha especie.
Calcule la concentración de en una disolución saturada de . Exprese el resultado en g/L.
Si , indique razonadamente cuál de los dos hidróxidos es más soluble en agua.
Ejercicio 3 · Opción A
3Opción A
1,4 puntosFormule o nombre los siguientes compuestos:
2,3-dimetilhexano
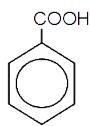
ácido benzoico
isopropil propil éter
Ejercicio 3 · Opción B
3Opción B
1,4 puntosFormule o nombre los siguientes compuestos:
butanona
ácido pentanodioico
vinilo
ciclobutino

Ejercicio 4 · Opción A
4Opción A
2,2 puntosSabiendo que la energía de activación para la reacción: es igual a , y para la reacción inversa su valor es :
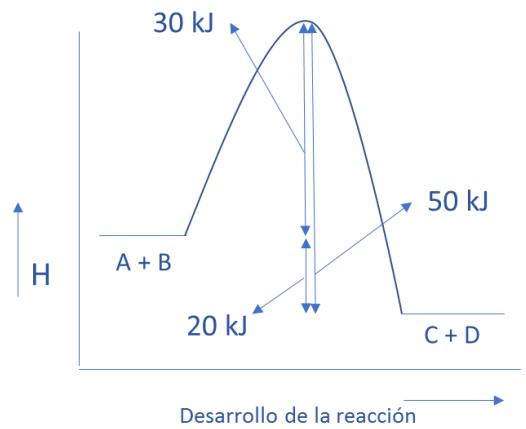
Indique justificadamente si la reacción directa será exotérmica o endotérmica.
Si la energía media de los productos de la reacción directa es igual a , ¿Cuál será la energía de los reactivos?
Justifique como afectaría la presencia de un catalizador a la energía de activación y al orden de la reacción directa.
Ejercicio 4 · Opción B
4Opción B
2,2 puntosSe dispone de de una disolución de un ácido débil de fórmula molecular AH, con una concentración . Si el grado de disociación es del :
Calcule la constante de acidez de la especie AH.
Calcule el pH de dicha disolución.
Justifique la veracidad o falsedad de la siguiente afirmación: “La base conjugada del ácido AH no sufre hidrólisis”.
Ejercicio 5 · Opción A
5Opción A
2,2 puntosSea la siguiente reacción de oxidación-reducción:
Ajústela por el método del ion-electrón.
Identifique justificadamente el agente oxidante y el agente reductor.
Ejercicio 5 · Opción B
5Opción B
2,2 puntosEn un recipiente de en el que se ha hecho vacío se introducen de y de . Se calienta la mezcla a estableciéndose el siguiente equilibrio:
Cuando se alcanza el equilibrio, el número de moles de es igual al de .
Calcule los moles de cada componente en el equilibrio.
Calcule y .
Razone como afectaría al equilibrio una disminución del volumen del sistema.
