Determina la entalpía estándar de combustión del naftaleno a partir de los datos de entalpías estándar de formación.
QuímicaBalearesPAU 2013Extraordinaria
Química · Baleares 2013
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosLa combustión completa del naftaleno genera dióxido de carbono y agua como se indica en la siguiente reacción química ajustada:
Calcula el volumen de dióxido de carbono que se genera en la combustión completa de de naftaleno, medido a y .
Ejercicio 1 · Opción B
1Opción B
2 puntosEl ácido benzoico (PM y ) es un buen conservante de alimentos. Determina el pH de una disolución de ácido benzoico de concentración .
Se tienen dos disoluciones separadas: una de cloruro de sodio y otra de acetato de sodio. ¿Cómo serán las disoluciones: ácidas, básicas o neutras? Razona la respuesta.
Ejercicio 2 · Opción A
2Opción A
2 puntosDada la siguiente reacción iónica redox:
Ajusta la reacción iónica por el método del ion-electrón.
¿Cuál es la especie oxidante?
Para valorar de sulfuro de sodio () se han utilizado de permanganato de potasio (). Determina la molaridad del permanganato empleado.
Ejercicio 2 · Opción B
2Opción B
2,5 puntosA el hidrogenocarbonato de sodio, , se descompone parcialmente según el equilibrio siguiente:
Se introducen de en un recipiente cerrado de de capacidad, en el cual previamente se ha hecho el vacío, y se calienta a hasta alcanzar el equilibrio químico.
Calcula el valor de a .
Calcula la presión total en el recipiente a la misma temperatura.
Si el volumen del recipiente fuese de , ¿cuántos moles de habría en el equilibrio?
Calcula el valor de de la siguiente reacción a :
Ejercicio 3 · Opción A
3Opción A
2,5 puntosNombra los siguientes ácidos: , y .
Considerando los valores de , a igual concentración, ¿qué ácido presenta una disolución acuosa con un menor valor de pH? Razona la respuesta.
Datos
El tiene una temperatura de ebullición de , mientras que el la tiene de . ¿Puedes explicar esta diferencia de temperaturas?
Ejercicio 3 · Opción B
3Opción B
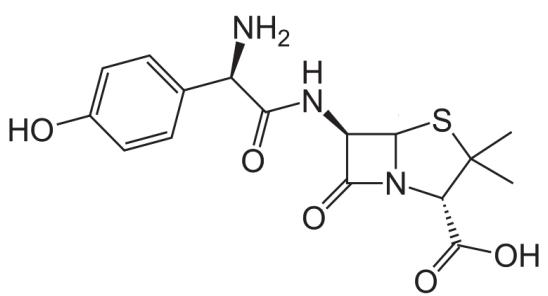
1 puntoEl Augmentine se utiliza para el tratamiento de infecciones bacterianas. Contiene amoxicilina y ácido clavulánico.
Indica el nombre de dos grupos funcionales presentes en la molécula de amoxicilina (ver la figura 1).
Cada comprimido de Augmentine contiene de amoxicilina () y de ácido clavulánico (ver la figura 2). Teniendo en cuenta que la posología habitual en un adulto es de un comprimido cada ocho horas durante una semana, ¿cuántos moles de amoxicilina habrá tomado un adulto durante esta semana?

Ejercicio 4 · Opción A
4Opción A
2,5 puntosEl tricloruro de fósforo reacciona con el cloro molecular para dar pentacloruro de fósforo, según la siguiente reacción:
Explica cómo se modificará el equilibrio si se aumenta la temperatura.
¿Es cierto que el equilibrio no se modifica por una disminución de la presión total? Razona la respuesta.
¿Se puede afirmar que la reacción es espontánea a cualquier temperatura? Razona la respuesta.
Explica la geometría y la polaridad de la molécula de .
Ejercicio 4 · Opción B
4Opción B
2,5 puntosEl dióxido de manganeso reacciona con el aluminio según la siguiente reacción ajustada:
Indica el número de oxidación del manganeso en las especies y .
¿Cuál es la especie oxidante? Razona la respuesta.
¿Cuál es la especie reductora? Razona la respuesta.
Calcula la energía que se desprende cuando se pone a reaccionar, en las mismas condiciones, de con de .
Ejercicio 5 · Opción A
5Opción A
1 puntoIndica el nombre y la utilidad del siguiente material de laboratorio:
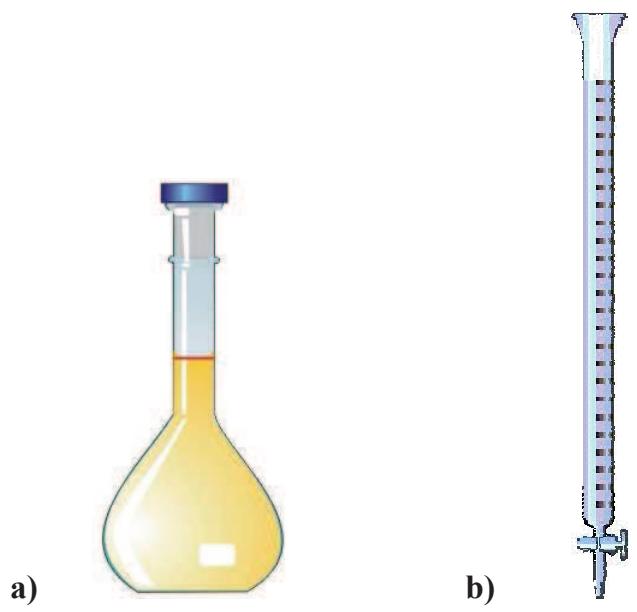
Ejercicio 5 · Opción B
5Opción B
2 puntosSean los siguientes compuestos: , y . Responde razonadamente a las preguntas siguientes:
¿Qué compuesto es soluble en benceno?
¿Qué fuerzas se deben superar para disolver en agua?
¿Qué fuerzas se deben superar para evaporar ?
¿Qué compuesto es el más duro de los tres?
