Justifique, haciendo los cálculos necesarios, que la reacción absorbe calor si se lleva a cabo a presión constante.
QuímicaCataluñaPAU 2017Extraordinaria
Química · Cataluña 2017
7 ejercicios90 min de duración
Ejercicio 1
1
2 puntosLa descomposición térmica del hidrogenocarbonato de sodio se utiliza en la fabricación de pan, porque el dióxido de carbono que desprende produce pequeñas burbujas en la masa y esto hace que «suba» cuando se pone el pan al horno. La reacción ajustada que tiene lugar es la siguiente:
Suponiendo que la reacción se efectúe a volumen constante, ¿la cantidad de calor absorbida será igual, mayor o más pequeña? Justifique la respuesta cualitativamente.
Nota: Suponga que la reacción se lleva a cabo siempre en condiciones estándar y a .
Ejercicio 2
2
2 puntosEn una actividad experimental, un grupo de alumnos disponen de una lámina de níquel y una de plata para montar una pila en condiciones estándar.
Diga qué otros reactivos y qué materiales necesitarán. Dibuje un esquema de la pila, y escriba las semirreacciones de cada electrodo y la reacción global.
El voltaje de funcionamiento de un LED va de a , aproximadamente. A partir de los valores de la tabla, justifique que el LED no podrá emitir luz si montan la pila con níquel y plata, e indique qué cambio deberían hacer en la pila para que el LED pueda emitirla.
| Par redox | ||||
| Potencial estándar de reducción, (V) |
Ejercicio 3
3
2 puntosLas soluciones parenterales son soluciones farmacológicas que se administran por medio de una inyección. Cuando se utiliza en el tratamiento de unos enfermos determinados, esta solución debe contener oligoelementos como, por ejemplo, el ion ; en este caso, es muy importante evitar la precipitación del hidróxido de cobre(II) en la sangre.
Escriba el equilibrio de solubilidad del hidróxido de cobre(II) y calcule su solubilidad a , expresada en .
Si el pH de la sangre es , calcule cuál es la concentración máxima de iones cobre(II) que puede haber en la sangre para evitar que precipite el hidróxido de cobre(II).
Ejercicio 4
4
2 puntosElija entre la cuestión 4 y la 5.
El dióxido de nitrógeno es un gas contaminante que se forma en las reacciones de combustión a alta temperatura. El dióxido de nitrógeno reacciona con el ozono presente en la atmósfera según la reacción química siguiente:
Varios estudios experimentales han concluido que, a una determinada temperatura, esta reacción sigue una cinética de primer orden respecto del dióxido de nitrógeno y también de primer orden respecto del ozono.
Escriba la ecuación de velocidad de la reacción. Explique razonadamente en qué unidades se expresan la velocidad de reacción y la constante de velocidad de esta reacción.
Para esta reacción se propone un mecanismo constituido por las dos etapas elementales siguientes:
1. (lenta)
2. (rápida)
Justifique que este mecanismo concuerda con los estudios experimentales cinéticos. A partir del modelo cinético de colisiones, explique razonadamente cuál de las dos etapas tendrá una energía de activación más alta y cómo influye la temperatura en la velocidad de la reacción.
Ejercicio 5
5
2 puntosElija entre la cuestión 4 y la 5.
Tenemos dos botellas, A y B, que contienen un líquido puro y transparente que puede corresponder a las sustancias orgánicas siguientes: etanoato de etilo () o ácido propanoico. Hemos sometido las muestras a la espectroscopia infrarroja para determinar qué sustancia hay en cada botella. Los espectros obtenidos son los siguientes:
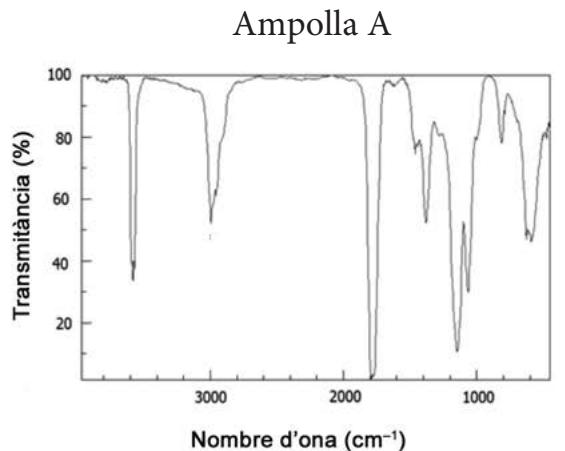
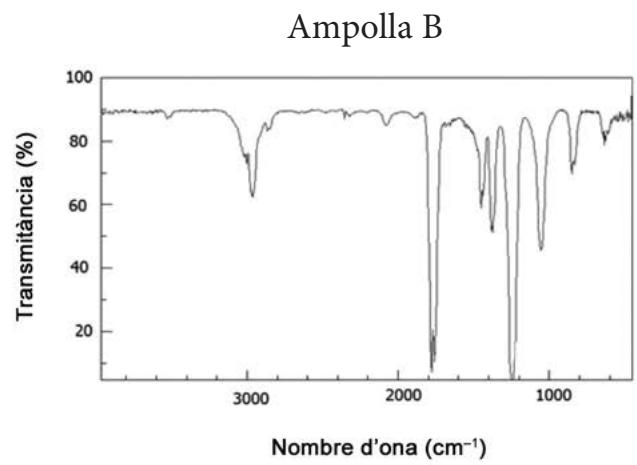
| Enlace | Intervalo de números de onda (cm) |
| C-O | 1 000-1 300 |
| C=O | 1 650-1 750 |
| C-H | 2 850-3 000 |
| O-H | 3 230-3 550 |
Explique qué le sucede a una molécula cuando absorbe radiación infrarroja. ¿Qué información proporciona la espectroscopia infrarroja? Identifique la sustancia orgánica que contiene cada botella y justifique la respuesta.
Otra técnica que se utiliza para identificar la estructura química de una molécula es la espectrometría de masas. Explique qué le sucede a una molécula cuando la sometemos a una espectrometría de masas. ¿Qué detectamos en un espectro de masas? ¿Qué información proporciona?
Ejercicio 6
6
2 puntosElija entre la cuestión 6 y la 7.
El naftaleno sólido, , se sublima en condiciones ambientales de presión y temperatura, y por eso se puede utilizar para fumigar espacios cerrados. El proceso de sublimación es el siguiente:
Introducimos de naftaleno en un recipiente cerrado de , a una temperatura de . Escriba la expresión de la constante de equilibrio en concentraciones () del equilibrio heterogéneo del proceso de sublimación del naftaleno, y calcule qué porcentaje en masa del naftaleno se habrá sublimado cuando se llegue al equilibrio.

¿De qué signo es la variación de entropía estándar () del proceso de sublimación del naftaleno? ¿Qué efecto tiene la temperatura en la espontaneidad de este proceso? Justifique las respuestas.
Ejercicio 7
7
2 puntosElija entre la cuestión 6 y la 7.
Algunas lejías de uso doméstico son soluciones acuosas que contienen un en masa de hipoclorito de sodio ().
Escriba la reacción de disociación del y justifique qué ion tendrá hidrólisis. Escriba la reacción de hidrólisis y calcule el pH de la lejía a .
¿Qué es una solución amortiguadora de pH? Justifique si la lejía puede actuar como solución amortiguadora de pH.
