¿Justifique, cuantitativamente, que esta reacción no será espontánea en condiciones estándar y a ? ¿A partir de qué temperatura lo sería, suponiendo que los valores de entalpía y de entropía estándar no varían con la temperatura?
QuímicaCataluñaPAU 2021Extraordinaria
Química · Cataluña 2021
7 ejercicios
Ejercicio 1
1
2,5 puntosEl monóxido de dinitrógeno u óxido nitroso () es conocido como gas hilarante o gas de la risa. Lo usan los dentistas como agente sedante, seguro y eficaz, para conseguir que el paciente se sienta más cómodo y relajado durante determinados procedimientos dentales. En ciertas condiciones, este óxido se puede descomponer según la reacción siguiente:
La descomposición en fase gaseosa del óxido nitroso se produce mediante el mecanismo de reacción siguiente, que consta de dos etapas elementales:
Etapa 1 (lenta):
Etapa 2 (rápida):
Dibuje, de una manera aproximada, un gráfico de la energía respecto a la coordenada de reacción; indique en el gráfico las energías de activación, los estados de transición y la variación de entalpía de la reacción global. A partir de las etapas del mecanismo de reacción, justifique que la reacción global es de primer orden.
Ejercicio 2
2
2,5 puntosEl 14 de enero de 2020 se produjo una gran explosión en una industria de Tarragona dedicada a la fabricación de óxido de etileno. Este producto químico se obtiene a partir de la oxidación del etileno con un exceso de oxígeno, empleando plata como catalizador, según la ecuación química siguiente:
En un reactor de , y a la temperatura de , conseguimos obtener de óxido de etileno haciendo reaccionar de etileno y de oxígeno en presencia de plata. Determine el valor de la constante de equilibrio en concentraciones () a . Diga si el valor de la constante de equilibrio en presiones () es igual o diferente que el valor de la constante de equilibrio en concentraciones a , y justifique la respuesta.
¿Tendremos un rendimiento de la reacción más favorable si la llevamos a cabo en un reactor de y a la temperatura de ? ¿Y si la llevamos a cabo en un reactor de y a la temperatura de ? Si mantenemos el volumen y la temperatura del reactor ( y ), pero no introducimos plata, ¿disminuiría la concentración de óxido de etileno cuando se alcanzara el equilibrio? Razone las respuestas.
Ejercicio 3
3
2,5 puntosPara tratar y conservar el agua de una piscina, podemos emplear un equipo comercial de depuración que consiste en un sistema de filtración al cual se añade un aparato de cloración salina que obtiene cloro por medio de la electrólisis de un producto natural como la sal común (cloruro de sodio).
A partir de la electrólisis del cloruro de sodio en solución acuosa obtenemos cloro gaseoso en el ánodo, mientras que en el cátodo el agua forma hidrógeno gaseoso e iones hidroxilo. Escriba e iguale las semirreacciones que tienen lugar en cada electrodo, así como la reacción global de este proceso electrolítico. Indique las polaridades de cada electrodo.
Un aparato comercial de cloración salina, adecuado para una piscina que contiene de agua, genera de cloro cada hora. ¿Qué intensidad de corriente debe pasar por la celda electrolítica?
Ejercicio 4
4
2,5 puntosLa tabla periódica actual está ordenada por el número atómico de los elementos químicos y nos aporta datos de propiedades como el radio atómico o iónico, la energía de ionización, la afinidad electrónica o la electronegatividad de los elementos, que varían de una manera regular en un grupo o en un periodo.
Defina los términos número atómico, energía de ionización, afinidad electrónica y electronegatividad de un elemento químico.
La primera energía de ionización de tres elementos químicos es , y . Sabemos que estos valores corresponden al magnesio, al potasio y al sodio, pero desconocemos qué valor corresponde a cada uno. Escriba la configuración electrónica de los tres elementos y justifique qué valor de la energía de ionización asignaría al magnesio y cuál al sodio. Compare razonadamente el radio del átomo de con el del ion .
Ejercicio 5
5
2,5 puntosEn una actividad llevada a cabo en el laboratorio para estudiar la solubilidad de diferentes carbonatos metálicos, un grupo de estudiantes realiza el experimento siguiente: transfieren a un vaso de precipitados de una solución de ; lentamente, mientras calientan un poco la solución, añaden de una solución de . Lo remueven bien, lo dejan enfriar hasta la temperatura ambiente () y observan que se ha formado un precipitado de color blanco de carbonato de calcio.
Justifique, a partir de los cálculos necesarios, la formación del precipitado. Considere aditivos los volúmenes de las soluciones acuosas.
Mediante un proceso de filtración, los estudiantes separan el precipitado de carbonato de calcio de la solución acuosa. De esta solución, hacen cuatro partes y las colocan en tubos de ensayo. Añaden al primer tubo una solución de , al segundo una solución de , al tercero una solución de ácido clorhídrico, y al cuarto tubo no añaden nada, pero lo calientan hasta . Explique razonadamente si en alguno de los cuatro tubos aparece un precipitado de carbonato de calcio.
Ejercicio 6
6
2,5 puntosEl etino (), llamado habitualmente acetileno, es el alquino más sencillo que existe y es bien conocida su utilización en equipos de soldadura. En este proceso, se pueden unir los bordes de dos piezas metálicas a la temperatura de fusión (aproximadamente, ) mediante el calor que genera la llama formada por la combustión del acetileno con oxígeno.
Escriba e iguale la reacción de combustión del acetileno gaseoso. ¿Qué cantidad de calor se desprenderá al quemar, a presión constante, de acetileno con de oxígeno, ambos gases medidos a y ?
Nota: Suponga que en la reacción de combustión se forma agua en estado líquido y dióxido de carbono en estado gaseoso.
Calcule la entalpía estándar de formación del acetileno gaseoso a . Razone si se desprende más calor en la formación de un mol de acetileno a presión constante o a volumen constante.
Ejercicio 7
7
2,5 puntosEn la elaboración casera del yogur a partir de la leche se utilizan bacterias, como el Lactobacillus bulgaricus, que producen ácido láctico, un ácido orgánico monoprótico.
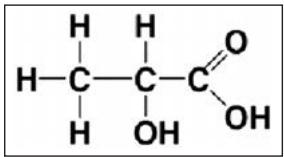
Un yogur contiene de ácido láctico. Calcule el pH del yogur a , considerando que el único ácido presente y responsable de su acidez es el ácido láctico.
Podemos determinar la cantidad de ácido láctico en un yogur por volumetría empleando hidróxido de sodio como solución valorante. En primer lugar, añadimos agua a una cantidad conocida de yogur; en segundo lugar, lo agitamos para homogeneizarlo, y, finalmente, iniciamos el proceso de valoración.
— Escriba la reacción de valoración.
— Explique cómo realizaría en el laboratorio esta valoración, e indique el material y otras sustancias que utilizaría.
