El premio Nobel de Química del año 2020 fue concedido a dos investigadoras, Emmanuelle Charpentier y Jennifer A. Doudna (figura 1), por el desarrollo de la técnica CRISPR-Cas9, o tijeras genéticas, la cual permite cortar el ADN en una posición concreta. Uno de los componentes estructurales del ADN es la desoxirribosa, que presenta la estructura química que se muestra en la figura 2:

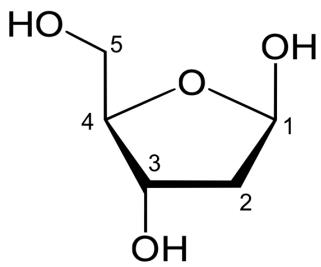
Calcula el peso molecular de la desoxirribosa.
¿Qué tipo de hibridación presenta el átomo de carbono indicado con el número 3 en la figura de la estructura química de la desoxirribosa? Justifica la respuesta.