En una serie de televisión, el actor Marc Smith ha aparecido muerto en su apartamento. La policía científica ha analizado una botella de agua que se encontraba cerca del cadáver y ha comprobado que estaba contaminada con cianuro de potasio (), en una concentración de M. La policía sabe que la dosis letal en personas es de mg por kg de masa corporal. Sabiendo que el actor pesa unos kg, ¿crees probable que la causa de la muerte fuese la ingesta de mL de agua envenenada con cianuro de potasio?
QuímicaBalearesPAU 2016Extraordinaria
Química · Baleares 2016
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
1 punto
El cianuro de potasio en contacto con el agua reacciona según el siguiente equilibrio químico, y se forma gaseoso, que es un compuesto muy tóxico:
Accidentalmente, se ha disuelto cianuro de potasio en agua. ¿Qué harías para disminuir la formación de , añadirías unas gotas de disolución de o de ? Razona la respuesta.
Ejercicio 1 · Opción B
1Opción B
2 puntosEl reacciona con el a según la reacción siguiente:
En un recipiente cerrado y vacío de L se introducen g de y la suficiente cantidad de . Una vez el sistema ha alcanzado el equilibrio químico a , la presión total es de atm y se han obtenido moles de agua.
Calcula la concentración de y de en el equilibrio químico.
¿Es cierto que para el equilibrio químico anterior ? Razona la respuesta.
Si se introduce en el recipiente un catalizador, ¿cómo afectará al equilibrio químico? Razona la respuesta.
Ejercicio 2 · Opción A
2Opción A
2,5 puntosSe añaden mL de una disolución M de a un matraz aforado y se enrasa con agua destilada hasta conseguir mL de disolución.
Determina el pH de la disolución diluida sabiendo que la constante de acidez vale .
Si se neutralizan mL de la disolución diluida de con mL de M, ¿cuántos moles de no habrán reaccionado?
¿Cómo se prepararían en el laboratorio mL de M a partir de sólido? Indica el material de laboratorio necesario para preparar esta disolución.
Ejercicio 2 · Opción B
2Opción B
2,5 puntosDada la siguiente reacción no ajustada:
Ajusta la reacción iónica por el método del ion-electrón.
Indica qué especie química actúa de oxidante.
Nombra los compuestos siguientes: y .
Ejercicio 3 · Opción A
3Opción A
2,5 puntosDetermina el valor de la variación de entalpía para la siguiente reacción no ajustada:
a partir de los datos siguientes:
Determina el calor que se debe aportar al sistema cuando reaccionan mL de (densidad g/mL) con g de agua para producir y .
¿Cuál de los siguientes elementos presenta un potencial de ionización mayor, el azufre o el oxígeno? Razona la respuesta.
Ejercicio 3 · Opción B
3Opción B
1,5 puntosCuando se hace reaccionar con un exceso de tiene lugar la reacción siguiente:
Contesta, de manera razonada, las preguntas siguientes:
¿Se puede afirmar que la variación de entropía de este proceso es positiva?
Sabiendo que la reacción directa de formación de presenta una energía de activación de kJ/mol, determina la energía de activación de la reacción inversa.
¿Es cierto que las reacciones exotérmicas tienen energías de activación negativas?
Ejercicio 4 · Opción A
4Opción A
2 puntosJustifica si son correctas o no las afirmaciones siguientes:
En la reacción , la molécula de oxígeno es la especie reductora.
Una pila formada por los electrodos de y tiene un potencial normal de V.
En una celda galvánica espontánea, el polo negativo recibe el nombre de cátodo.
Cuando se introduce una lámina de plomo dentro de un vaso de precipitados que contiene una disolución de , no tiene lugar ningún proceso redox espontáneo.
Ejercicio 4 · Opción B
4Opción B
2 puntosUn elemento A es el alcalinotérreo del tercer período; mientras que un elemento B es el halógeno del segundo período.
Escribe la configuración electrónica del ion más estable del elemento A.
¿Podemos afirmar que el radio atómico del elemento B es mayor que el del anión ? Razona la respuesta.
¿Qué elemento tiene una menor afinidad electrónica, el A o el B? Razona la respuesta.
¿Es cierto que el ion y el elemento A son isoelectrónicos? Razona la respuesta.
Ejercicio 5 · Opción A
5Opción A
2 puntosSean los siguientes compuestos químicos: y
¿Qué tipo de enlace químico presentan las moléculas anteriores? Razona la respuesta.
De los compuestos químicos anteriores, ¿hay alguno que conduzca la corriente eléctrica en estado fundido? Razona la respuesta.
Justifica la geometría de la molécula de mediante el modelo de la repulsión de pares de electrones de la capa de valencia.
Ejercicio 5 · Opción B
5Opción B
2 puntosEn un laboratorio se dispone de dos disoluciones separadas de y .
¿Cómo son estas disoluciones: ácidas, básicas o neutras? Razona la respuesta.
¿Cómo gestionarías el residuo de ? ¿Lo neutralizarías con un ácido diluido o simplemente se podría verter por el fregadero? Razona la respuesta.
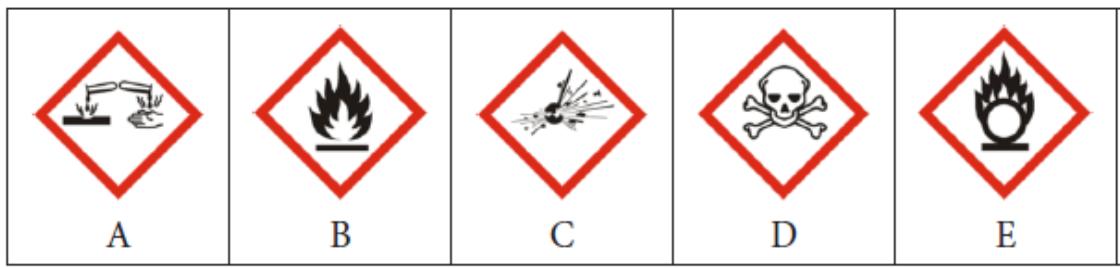
La ficha de seguridad química del indica que es comburente. De los pictogramas que aparecen en la figura 2 (A-E) indica el que debe aparecer en la etiqueta de este compuesto químico.