¿Cuál es la concentración máxima de iones (expresada en mol L) que puede contener el agua para que no se produzca un precipitado de fluoruro de calcio?
QuímicaCataluñaPAU 2013Extraordinaria
Química · Cataluña 2013
7 ejercicios90 min de duración
Ejercicio 1
1
2 puntosLa fluoración del agua potable consiste en la adición limitada y controlada de iones fluoruro en el sistema público de agua potable, con el objetivo de reducir el riesgo de caries dental de la población, aunque actualmente se discute su efectividad. Este fluoruro se añade habitualmente en forma de fluoruro de sodio hasta tener una concentración de mol L de fluoruro. Cuando el agua potable de una ciudad es dura, porque contiene mucha cantidad de iones , puede precipitar el fluoruro de calcio.
Si se nos forma un precipitado de g de fluoruro de calcio, ¿qué cantidad mínima de agua pura necesitaremos añadir para disolverlo?
Ejercicio 2
2
2 puntosLa tabla siguiente muestra los datos de dos propiedades del sodio, el magnesio y el azufre:
A partir de la configuración electrónica de los átomos, y utilizando el modelo atómico de cargas eléctricas:
| Na | Mg | S | |
| Radio atómico (nm) | 0,156 | 0,136 | 0,104 |
| Primera energía de ionización (kJ mol-1) | 492 | 743 | 1003 |
Explique razonadamente la variación del radio atómico y la variación de la primera energía de ionización en estos tres elementos.
Diga qué valor cabe prever para la segunda energía de ionización del magnesio en relación con su primera energía de ionización. ¿El radio del ion sulfuro () será más pequeño o más grande que el radio del átomo de azufre? Justifique las respuestas.
Ejercicio 3
3
2 puntosUna marca de envases de bebidas ha patentado una lata que permite obtener bebidas frías o calientes en cualquier lugar y a cualquier hora del día. El envase consta de dos recipientes superpuestos: el recipiente externo de aluminio contiene la bebida y el recipiente interno contiene unas sustancias que entran en contacto en el momento que abrimos el envase, sin mezclarse con la bebida en ningún momento. En función de qué sustancias haya en el recipiente interno, la bebida se enfriará o se calentará.

Suponga que la sustancia que contiene el recipiente interno de la lata es un sólido que se disuelve con agua en el momento de abrir el envase. ¿Qué sustancia de la tabla siguiente elegiría a la hora de diseñar la lata, si quiere enfriar la bebida? ¿Y si la quiere calentar? Justifique las respuestas.
| Sustancia | CaCl2 | Na2CO3 | KOH | NaCl | NH4NO3 | NH4Cl |
| Entalpía estándar de solución (ΔHsol°), a 25°C (kJ g-1) | -8878 | -3053 | -774 | +228 | +491 | +776 |
Explique el procedimiento experimental que seguiría en el laboratorio para obtener la entalpía de solución del en agua e indique el material que utilizaría y las medidas experimentales que habría que determinar.
Ejercicio 4
4
2 puntosElija entre la cuestión 4 y la 5.
La tioacetamida es un compuesto orgánico, de fórmula , que se utiliza en síntesis orgánica e inorgánica como fuente de sulfuro. La tioacetamida reacciona con agua, en un medio ácido, para formar sulfuro de hidrógeno:
La ecuación de la velocidad de esta reacción viene dada por la expresión siguiente:
Indique el orden total de la reacción. ¿Con qué unidades se expresa la velocidad de una reacción química? ¿Qué unidades tiene la constante de velocidad de la reacción de la tioacetamida con agua en un medio ácido? Justifique todas las respuestas.
Tenemos una solución acuosa que contiene y es M en . Justifique si la velocidad de la reacción aumentará o disminuirá si añadimos un poco de a la solución, o si sustituimos el ácido clorhídrico por ácido acético de la misma concentración.
Ejercicio 5
5
2 puntosElija entre la cuestión 4 y la 5.
El ácido butanoico, llamado habitualmente ácido butírico, se utiliza en la obtención de compuestos que se usan en jarabes.
Hemos preparado en el laboratorio una solución acuosa de este ácido y el pH medido experimentalmente ha sido .

Escriba la reacción del ácido butírico con agua. ¿Cuál era la concentración inicial de la solución acuosa de ácido butírico?
¿Qué es una solución amortiguadora de pH? ¿Qué tendríamos que añadir a la solución de ácido butírico para tener una solución amortiguadora de pH? Justifique la respuesta.
Ejercicio 6
6
2 puntosElija entre la cuestión 6 y la 7.
Un químico de una empresa del sector energético estudia la conversión del metano en otros combustibles, concretamente la reacción del metano con vapor de agua para formar hidrógeno:
El químico está interesado en optimizar la concentración de hidrógeno cuando se alcanza el estado de equilibrio. Inicialmente inyecta de manera simultánea mol de cada gas (, , y ) en un reactor de L que se mantiene a K.
Justifique, mediante los cálculos necesarios, en qué dirección avanzará la reacción para alcanzar el equilibrio.
Una vez alcanzado el equilibrio, y para mejorar el rendimiento de la reacción, el investigador puede modificar el volumen o la temperatura del reactor. ¿Le conviene aumentar o disminuir el volumen? ¿Le conviene aumentar o disminuir la temperatura? Explique razonadamente las respuestas.
Ejercicio 7
7
2 puntosElija entre la cuestión 6 y la 7.
Muchas monedas encontradas en excavaciones arqueológicas son de cobre y, habitualmente, están corroídas. Un procedimiento para limpiarlas consiste en colgarlas de un hilo de cobre, sumergirlas en una solución acuosa de , añadir un electrodo de grafito a la solución y conectar el hilo de cobre y el grafito a una pila, como se observa en la figura. La reacción iónica global que se produce es la siguiente:
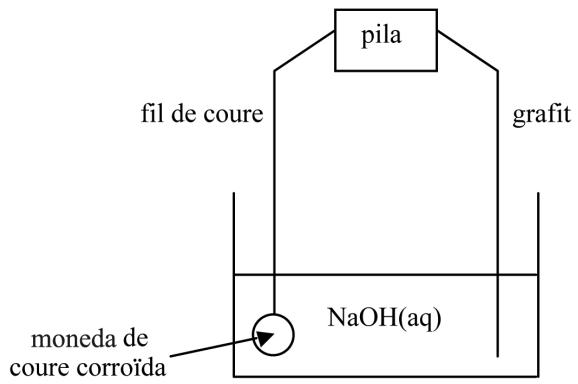
Escriba las semirreacciones que tendrán lugar en cada uno de los electrodos durante el proceso de limpieza de la moneda de cobre corroída e indique el nombre y la polaridad de los electrodos. ¿Por qué es necesario unir el hilo de cobre y el grafito con una pila?
Explique en qué consiste el proceso de corrosión de un metal e indique los factores ambientales que lo producen. Indique a partir de qué criterio deducimos qué metal se corroerá más fácilmente, de una serie de metales sometidos a las mismas condiciones ambientales y durante el mismo tiempo.
