i) Determina el valor de la constante de equilibrio a .
ii) A partir de los valores de la tabla 1, ¿se puede deducir si la reacción de disociación del es un proceso endotérmico? Razona la respuesta.
QuímicaBalearesPAU 2020Extraordinaria
Química · Baleares 2020
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosEl es un gas abundante en la Tierra, indispensable para la fotosíntesis de las plantas. En un laboratorio de Química, se ha estudiado el efecto de la temperatura sobre la reacción de disociación de según la reacción química ajustada siguiente:
Un químico ha rellenado algunas de las celdas de la tabla 1, donde se indican a tres temperaturas los valores de las concentraciones de reactivos y productos una vez alcanzado el equilibrio químico y el valor de algunas constantes de equilibrio.
| Temperatura, °C | [CO2]eq, M | [CO]eq, M | [O2]eq, M | K, mol1/2·L-1/2 |
| 1500 | 0,048 | |||
| 2000 | 0,10 | 0,20 | 0,25 | |
| 2500 | 0,0025 | 0,10 | 0,20 | 17,6 |
Formula los compuestos siguientes: ácido carbónico y dietilamina.
Ejercicio 1 · Opción B
1Opción B
2 puntosNombra los compuestos siguientes: y .
Explica el tipo de hibridación que presentan los átomos de carbono en la molécula .
¿Qué tipo de enlace químico presenta la molécula ? Justifica la respuesta.
Ejercicio 2 · Opción A
2Opción A
2 puntosLa siguiente reacción química ajustada corresponde a un proceso redox:
Identifica la especie oxidante. Justifica la respuesta.
Calcula el volumen de que se obtendrá haciendo reaccionar de con un exceso de ácido sulfúrico, a de temperatura y a una presión de .
Indica de forma razonada si la reacción siguiente corresponde a un proceso redox:
Ejercicio 2 · Opción B
2Opción B
2 puntosEn el siglo pasado, el científico alemán Fritz Haber diseñó un proceso para obtener amoníaco a partir de la fijación del nitrógeno del aire, en el cual ocurre la reacción ajustada siguiente:
En un recipiente cerrado y vacío de , se introducen de , de y de a .
Justifica por qué el sistema no está en equilibrio y explica de forma razonada el sentido hacia donde se desplazará la reacción para alcanzarlo.
Una vez alcanzado el equilibrio, ¿se obtendrá más amoníaco si se disminuye el volumen del recipiente? Justifica la respuesta.
Calcula el valor de a .
Ejercicio 3 · Opción A
3Opción A
2 puntosEscribe la configuración electrónica de los iones y . ¿Cuál de los iones anteriores presenta mayor estabilidad? Razona la respuesta.
Los valores de las energías reticulares de los compuestos y son, respectivamente, y . Justifica la diferencia entre los valores de la energía reticular de los compuestos y .
Explica la geometría de la molécula según la TRPECV.
Ejercicio 3 · Opción B
3Opción B
2 puntosIndica de manera razonada si las afirmaciones siguientes son verdaderas o falsas:
El radio atómico del bromo es menor que el del calcio.
El fósforo presenta dos electrones desapareados en su estado fundamental.
La combinación de números cuánticos está permitida.
El flúor es el halógeno con mayor electronegatividad del grupo 17 de la tabla periódica.
Ejercicio 4 · Opción A
4Opción A
2 puntosEn un laboratorio se han preparado dos disoluciones por separado de y . Sin hacer ningún cálculo numérico, indica de forma razonada si estas disoluciones son ácidas, básicas o neutras.
Datos
¿Qué cantidad (en gramos) de se debe utilizar para neutralizar completamente de una disolución de ?
Indica el material de laboratorio necesario para llevar a cabo una valoración ácido-base.
Ejercicio 4 · Opción B
4Opción B
2 puntosEl ácido fluorhídrico (HF) es una sustancia tóxica y corrosiva. La constante de acidez de este ácido, a , es .
¿Qué volumen de HF comercial, del en peso y densidad , se necesita para preparar de una disolución de HF ?
¿Cuál es el pH de una disolución de HF a ?
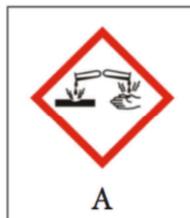
Indica los dos pictogramas de la figura siguiente (A-E) que deben aparecer en la etiqueta de la botella de ácido fluorhídrico. Justifica la respuesta.




Ejercicio 5 · Opción A
5Opción A
2 puntosLa ecuación de velocidad del proceso es .
Indica de manera razonada si las siguientes afirmaciones son correctas:
La velocidad de reacción sigue una cinética de primer orden respecto al producto C.
Cuando se duplica la concentración de B en el proceso anterior, la velocidad también se duplica.
El valor numérico de la constante de velocidad no varía con la temperatura.
La velocidad de reacción depende del estado físico de los reactivos.
Ejercicio 5 · Opción B
5Opción B
2 puntosPara determinar cuantitativamente el contenido de hierro que contiene una muestra, esta se disuelve en ácido y se lleva a cabo la valoración del ion empleando una solución de permanganato de potasio de concentración conocida. La reacción de valoración que tiene lugar es la siguiente:
Ajusta la reacción iónica utilizando el método del ion-electrón.
Indica, de forma razonada, cuál de los reactivos actúa como reductor.
¿Es espontánea la reacción anterior en condiciones estándar? Justifica la respuesta.
