Dibuje un esquema de la célula electrolítica, indicando el polo positivo, el polo negativo y el flujo de electrones durante el proceso de electrolisis. Escriba las reacciones que se producen en el ánodo y en el cátodo.
QuímicaAsturiasPAU 2016OrdinariaVariante 2
Química · Asturias 2016
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2,5 puntosConstruya el ciclo de Born-Haber para la formación del , a partir de bromo líquido y sodio metálico, y calcule la energía de red del compuesto, a partir de los siguientes datos:
Ejercicio 1 · Opción B
1Opción B
2,5 puntosDetermine si se formará precipitado cuando a de agua destilada se añaden de disolución acuosa de sulfato de sodio, , y de nitrato de plomo(II), , sólido. Suponga que los volúmenes son aditivos y que el volumen del sólido puede despreciarse.
Ejercicio 2 · Opción A
2Opción A
2,5 puntosEn el proceso de purificación del mediante electrolisis, una lámina de impuro actúa como ánodo de la célula electrolítica y una lámina de de elevada pureza actúa como cátodo. Ambas están sumergidas en una disolución ácida de .
Calcule el tiempo que tiene que estar funcionando la célula para que la masa del cátodo aumente en al pasar una corriente de .
Ejercicio 2 · Opción B
2Opción B
2,5 puntosCalcule el pH de la disolución que se obtiene al añadir a de agua destilada, de disolución acuosa de hidróxido de bario, , y de . Suponga que los volúmenes son aditivos.
Ejercicio 3 · Opción A
3Opción A
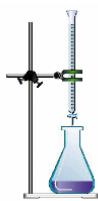
1 puntoEn el laboratorio se dispone del dispositivo experimental de la figura y del material de laboratorio y reactivos que se relacionan: pipeta aforada de , disolución acuosa titulada de , muestra de vinagre comercial e indicador.
Indique el procedimiento experimental a seguir para realizar la determinación del contenido de ácido acético en un vinagre comercial.
Ejercicio 3 · Opción B
3Opción B
1 puntoDibuje un esquema de la pila Daniell e indique el material de laboratorio y los reactivos utilizados para su construcción.
Ejercicio 4 · Opción A
4Opción A
2 puntosJustifique la siguiente relación de radios: .
Datos
Deduzca la estructura de Lewis para el metanal, . Nombre y dibuje su geometría molecular e indique los ángulos de enlace aproximados.
Datos
Ejercicio 4 · Opción B
4Opción B
2 puntosLas siguientes configuraciones electrónicas:
i)
ii)
representan estados excitados de los átomos. Para cada caso, escriba la configuración electrónica del estado fundamental e indique el período de la tabla periódica al que pertenece cada elemento.
Justifique las variaciones observadas en los valores de las temperaturas de ebullición de las siguientes sustancias a :
| Compuesto | |||
| Temperatura de ebullición (°C) |
Ejercicio 5 · Opción A
5Opción A
2 puntosCalcule el número de moles de disueltos en de una disolución acuosa saturada de la sal a .
Datos
Escriba las fórmulas semidesarrolladas y nombre los isómeros geométricos del 1,2-dicloro-1-buteno.
Ejercicio 5 · Opción B
5Opción B
2 puntosDetermine el intervalo de temperaturas (altas o bajas) en el que la reacción:
es espontánea.
Escriba las fórmulas semidesarrolladas de los siguientes compuestos:
i. 1,3,5-tribromo-2-penteno
ii. Dietilamina
iii. 2-butanol
iv. Butanoato de metilo
