Indique los números cuánticos que describen el orbital en donde se encuentra el electrón diferenciador del elemento Y, explicando su decisión y represente dicho orbital.
QuímicaNavarraPAU 2023Extraordinaria
Química · Navarra 2023
10 ejercicios
Ejercicio 1 · Opción A
1Opción A
2 puntosLa configuración electrónica en su estado fundamental del elemento X es y la del elemento Y es .
Justifique los iones que formarán preferentemente X e Y, así como el tipo de enlace que se establecerá cuando se combinen, indicando la fórmula del compuesto formado.
Justifique qué elemento presentará un mayor radio atómico.
Ejercicio 1 · Opción B
1Opción B
2 puntosConsidere las moléculas: , , y .
Describa y justifique la hibridación de los átomos centrales de las siguientes moléculas: , , y .
Justifique en dichas moléculas su momento dipolar e indique si alguna de ellas podría formar puentes de hidrógeno.
Ejercicio 2 · Opción A
2Opción A
2 puntosEn un recipiente de 2 litros a se introducen moles de y moles de . Sabiendo que a esa temperatura el valor de es para la reacción :
Justifique en qué sentido evolucionará la reacción hasta alcanzar el equilibrio.
Calcule las concentraciones de las dos sustancias en el equilibrio.
El tetraóxido de dinitrógeno es un gas incoloro, mientras que el dióxido de nitrógeno tiene un color rojizo. Si introducimos el recipiente con la mezcla de los dos gases en equilibrio en un baño de agua y hielo, la mezcla va perdiendo color. Por el contrario, si introducimos el recipiente en un baño a , la mezcla toma un color más rojizo. Justifique si la reacción en sentido directo es endotérmica o exotérmica.
Ejercicio 2 · Opción B
2Opción B
2 puntosConsidere el equilibrio de solubilidad del yoduro de plomo (II).
Escriba el equilibrio de disociación del yoduro de plomo (II) y la expresión de su constante de solubilidad.
Calcule la solubilidad del yoduro de plomo en agua.
Justifique qué efecto tendría en la solubilidad del yoduro de plomo añadir yoduro sódico, que se disocia completamente, a la disolución.
Indique si en una disolución acuosa con una concentración M de iones yoduro y M de iones se observará formación de precipitado de yoduro de plomo.
Ejercicio 3 · Opción A
3Opción A
2 puntosSe valoraron mL de una disolución acuosa de amoniaco con una disolución acuosa de ácido acético M alcanzándose el punto de equivalencia tras añadir mL de dicha disolución ácida.
Indique todos los equilibrios presentes tanto en la disolución inicial de amoniaco como en la disolución inicial de ácido acético.
Calcule el pH de la disolución inicial de amoniaco.
Justifique el carácter ácido, básico o neutro de la disolución en el punto de equivalencia.
Ejercicio 3 · Opción B
3Opción B
2 puntosEn mL de una disolución acuosa de ácido benzoico se midió un pH de .
Determine la concentración inicial de ácido benzoico en la disolución.
Calcule el grado de disociación del ácido benzoico en dicha disolución.
Calcule el volumen de una disolución acuosa de hidróxido sódico M necesario para neutralizar esta disolución de ácido benzoico.
Justifique si en el punto de equivalencia el pH será ácido, básico o neutro.
Ejercicio 4 · Opción A
4Opción A
2 puntosEl aluminio metal se obtiene industrialmente por electrólisis de óxido de aluminio (bauxita) fundido, utilizando electrodos de grafito.
Escriba las ecuaciones químicas que tendrán lugar en el cátodo y en el ánodo indicando la polaridad de los mismos.
Calcule cuánto tiempo debe circular una corriente de A para depositar g de aluminio.
Calcule el volumen de oxígeno que se desprenderá medido a y atm de presión.
Ejercicio 4 · Opción B
4Opción B
2 puntosEl permanganato potásico es un potente oxidante.
Justifique si, en condiciones estándar, se producirá la oxidación de una pieza de cobre al sumergirla en una disolución de permanganato potásico que contiene ácido sulfúrico, para producir sulfato de manganeso (II), sulfato de cobre (II) y agua.
Ajuste, utilizando el método ion-electrón, la ecuación redox correspondiente.
Calcule cuántos gramos de cobre podrían oxidarse, de producirse dicha reacción, empleando mL de una disolución M de permanganato potásico.
Ejercicio 5 · Opción A
5Opción A
2 puntosConsidere los compuestos orgánicos butanal, butan-2-ol, Z-pent-2-eno y E-pent-2-eno.
Formule los siguientes compuestos químicos: butanal, butan-2-ol, Z-pent-2-eno, E-pent-2-eno.
Indique si algunos de los compuestos anteriores son isómeros entre sí y el tipo de isomería que presentan.
Justifique si alguno de los compuestos anteriores puede presentar isomería óptica. En caso afirmativo, represente ambos isómeros ópticos.
Ejercicio 5 · Opción B
5Opción B
2 puntosEl poliestireno y el PET (polietilenterftalato) son dos polímeros orgánicos que se utilizan comúnmente en la fabricación de envases.
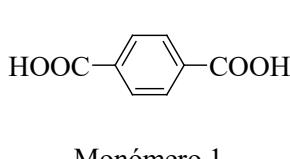
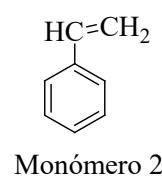
Identifique para poliestireno y PET cuáles son los monómeros que se emplean de entre los representados.
Proponga una estructura para cada uno de estos polímeros.
Explique qué tipo de reacción se emplea para la síntesis de cada uno de estos polímeros.
