Calcular la constante .
QuímicaPaís VascoPAU 2022Ordinaria
Química · País Vasco 2022
10 ejercicios90 min de duración
Datos generales del examen
Ejercicio 1
1
2,5 puntosBLOQUE AProblemas
Responda a 2 de los 4 problemas del Bloque A.
Se introducen de cloruro de nitrosilo (NOCl) en un matraz de y el recipiente se calienta a . El cloruro de nitrosilo se disocia un según la ecuación:
Calcular la constante .
¿Cómo cambia (aumenta, disminuye o no se altera) la concentración de si se añade un gas inerte (Ar) a la mezcla en equilibrio del matraz a volumen y temperatura constante? Justificar.
Ejercicio 2
2
2,5 puntosBLOQUE AProblemas
Responda a 2 de los 4 problemas del Bloque A.
Una disolución de de un ácido (AH) en de agua se valora con alcanzándose el punto de equivalencia tras añadir de la base. Calcular:
La molaridad del ácido AH en la disolución inicial.
El pH de la disolución inicial de AH si su constante de ionización es .
El grado de ionización porcentual de AH en la disolución inicial.
La masa molar del ácido AH en g/mol.
Ejercicio 3
3
2,5 puntosBLOQUE AProblemas
Responda a 2 de los 4 problemas del Bloque A.
A el producto de solubilidad del cromato de plata () en agua es y el del cloruro de plata () es .
Calcular los gramos de cromato de plata disueltos en litros de agua a .
Se preparan otros litros con una disolución saturada de cloruro de plata a . Calcular los gramos de plata que contiene.
¿Cuál de las dos disoluciones anteriores tiene más plata disuelta?
¿Cuál de las dos sales es más insoluble en gramos/Litro?
Ejercicio 4
4
2,5 puntosBLOQUE AProblemas
Responda a 2 de los 4 problemas del Bloque A.
Dada la reacción química:
Ajustar la reacción empleando el método del ión-electrón.
Indicar razonadamente qué especie se oxida y qué especie se reduce.
¿Cuántos mL de harán falta para reaccionar con de gaseoso medidos a y ?
Ejercicio 5
5
2 puntosBLOQUE BCuestiones
Responda a 1 de las 2 cuestiones del Bloque B.
Escribir un ejemplo de ecuación química para cada una de las siguientes transformaciones, formulando y nombrando todos los reactivos y productos:
Adición de a un alqueno de 3 átomos de carbono.
Oxidación suave de un alcohol primario de 4 átomos de carbono.
Condensación de un ácido carboxílico de 2 átomos de carbono y un alcohol de 3 átomos de carbono.
Reacción de con un hidrocarburo aromático de 6 átomos de carbono.
Ejercicio 6
6
2 puntosBLOQUE BCuestiones
Responda a 1 de las 2 cuestiones del Bloque B.
La valoración de vinagres comerciales se hace empleando un montaje como el de la imagen:
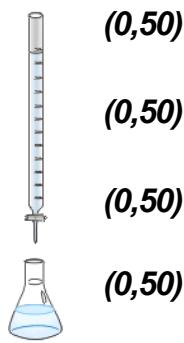
Nombrar todo el material necesario, completar el montaje experimental e indicar qué sustancia(s) se coloca(n) en cada elemento del montaje.
Escribir la ecuación química ajustada de la reacción, nombrar un indicador adecuado y describir brevemente el procedimiento operativo.
En el punto de equivalencia, el pH ¿será neutro, ácido o básico? Razonar.
Si en lugar de vinagre se valorase una disolución acuosa de , ¿cómo sería el pH en el punto de equivalencia? Razonar.
Ejercicio 7
7
1,5 puntosBLOQUE CCuestiones
Responda a 2 de las 4 cuestiones del Bloque C.
Dados los siguientes grupos de números cuánticos :
Indicar cuáles no son permitidos. Razonar por qué.
Señalar los orbitales atómicos correspondientes a los permitidos.
Identificar el elemento químico con un electrón de valencia en el orbital .
Ejercicio 8
8
1,5 puntosBLOQUE CCuestiones
Responda a 2 de las 4 cuestiones del Bloque C.
Con los datos de los potenciales normales de reducción:
Razonar si será espontánea la reacción:
¿Se formará hidrógeno gaseoso al introducir estaño metálico en (aq) ?
Dibuja la notación de la pila con electrodos de estaño y cobre. Escribe las reacciones químicas que ocurrirán en el ánodo y el cátodo.
Ejercicio 9
9
1,5 puntosBLOQUE CCuestiones
Responda a 2 de las 4 cuestiones del Bloque C.
Teniendo en cuenta las estructuras de Lewis y las geometrías de estas moléculas y razonando las respuestas: , , ,
Seleccionar los compuestos que son apolares en estado gaseoso.
Seleccionar un compuesto con enlaces iónicos.
Comparando y , ¿cuál tendrá un punto de ebullición mayor?
Ejercicio 10
10
1,5 puntosBLOQUE CCuestiones
Responda a 2 de las 4 cuestiones del Bloque C.
Razonar si son ciertas o falsas las siguientes afirmaciones suponiendo que los valores termodinámicos de la siguiente reacción no varían con la temperatura:
La reacción será espontánea a cualquier temperatura.
La reacción no será espontánea a ninguna temperatura.
Habrá una temperatura a la cual la reacción pasará de ser no espontánea a espontánea. En caso de existir, calcular dicha temperatura.
