Indique su nombre y símbolo atómico, así como su posición (grupo y periodo) en la Tabla Periódica. ¿Cómo se suele denominar a ese grupo?
QuímicaMurciaPAU 2023Extraordinaria
Química · Murcia 2023
10 ejercicios
Ejercicio 1
1
2 puntosDado el elemento con configuración electrónica :
Explique brevemente si las siguientes configuraciones electrónicas corresponden a un átomo excitado de dicho elemento, a un ion de dicho elemento o si no son posibles:
Escriba un posible conjunto de números cuánticos para un electrón .
¿Cuántos electrones de valencia, y cuántos electrones desapareados, tendrá este elemento, en su estado fundamental? Justifique brevemente su respuesta.
Indique entre los siguientes, qué conjunto de estados de oxidación más probables corresponde a este elemento:
i)
ii)
iii)
Ejercicio 2
2
2 puntosDibuje el ciclo de Born-Haber para la formación del a partir de y , y determine su entalpía de formación, a partir de los siguientes datos:
Datos
Explique la diferencia de signo entre la primera y la segunda afinidad electrónica del .
Ejercicio 3
3
2 puntosObserve atentamente el siguiente diagrama entálpico (perfil de reacción) y conteste a las preguntas:
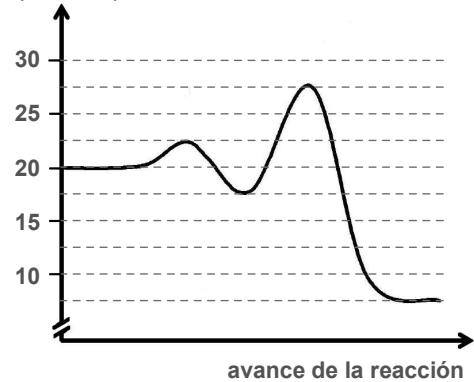
¿En cuántas etapas ocurre la reacción representada?
Indique el valor numérico de la de cada etapa.
¿Cuántos estados de transición hay en esta reacción y cuál es la energía de cada uno de ellos?
¿Qué etapa es la determinante de la velocidad de la reacción? Explique en qué se basa su respuesta.
Calcule el valor de para la reacción directa y explique si dicha reacción es exotérmica o endotérmica.
Explique si la adición de un catalizador efectivo afectará a la velocidad de la reacción global y a su .
Ejercicio 4
4
2 puntosEn un recipiente cerrado a se encuentran de grafito en equilibrio con una mezcla de y , según la siguiente reacción:
Calcule la presión parcial de cada gas sabiendo que la en el equilibrio es de .
Calcule el valor de para dicho equilibrio, a .
Explique cómo variará la presión parcial de en los siguientes casos:
Si se adicionan al recipiente otros de grafito.
Si mediante un émbolo se reduce el volumen del recipiente.
Ejercicio 5
5
2 puntosEscriba los procesos ácido-base (disociación, hidrólisis) que tienen lugar al disolver las siguientes sustancias en agua, indicando adecuadamente si se trata o no de un equilibrio, y cómo será el pH de la disolución resultante (neutro, ácido o básico): i) ; ii) ; iii) ; iv) ; v) .
Indique cuál de las disoluciones anteriores será más ácida, y cuál más básica (suponiendo que se parte de cantidades equimolares de las sustancias).
Ejercicio 6
6
2 puntosCalcule el grado de disociación de una disolución acuosa de () de concentración .
El pH de una disolución de un ácido monoprótico (HA), de concentración es . Explique numéricamente si se trata de un ácido fuerte o débil.
Calcule la concentración de aniones hidroxilo, , en la disolución del apartado b).
Ejercicio 7
7
2 puntosDada la siguiente reacción de oxidación-reducción (sin ajustar):
Indique cuál es el agente oxidante y el reductor, y cómo varían sus estados de oxidación.
Ajuste la reacción mediante el método del ion-electrón.
Ejercicio 8
8
2 puntosConsidere una pila galvánica formada por un electrodo de sumergido en una disolución acuosa de y por un electrodo de sumergido en una disolución acuosa de .
Explique cuál de los electrodos actuará como cátodo y cuál como ánodo. Escriba las semirreacciones que tienen lugar en cada uno de ellos, identificándolas como oxidación o reducción, y escriba también la reacción global de la pila.
Calcule la fuerza electromotriz de la pila, y la variación de energía libre.
Explique brevemente si en este proceso se produce o se consume electricidad.
Razone si durante la reacción varía (y cómo) la masa de los electrodos.
Ejercicio 9
9
2 puntosEscriba las fórmulas semidesarrolladas de los siguientes pares de compuestos e indique el tipo y subtipo de isomería que presentan entre sí:
i) etil vinil éter y alil metil éter
ii) but-1-eno y ciclobutano
Indique el tipo y subtipo de isomería que presentan los siguientes pares de compuestos:
Pareja de enantiómeros de un derivado de ciclohexano.
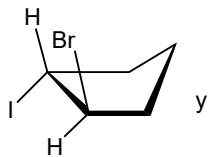
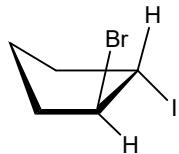
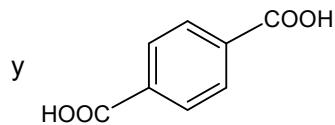
Ácido orto-ftálico y ácido para-ftálico.
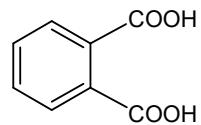
Indique el tipo de reacción orgánica (una sola palabra es suficiente):
Nombre las dos sustancias orgánicas que intervienen en la reacción anterior.
Ejercicio 10
10
2 puntosFormule o nombre:
i) estireno
ii)
iii) 3-metilpentanamida
Dado el compuesto :
Nómbrelo.
Explique si puede presentar algún tipo de isomería espacial (geométrica y/u óptica).
Escriba la fórmula semidesarrollada de un isómero estructural de función.
Escriba la ecuación química para la reacción de combustión del compuesto con .
Complete la siguiente reacción, con todos los productos mayoritarios esperados:
