5
2 puntosLa hidrólisis de la sacarosa, o azúcar de mesa, se puede efectuar en un medio ácido que actúa como catalizador. Se ha comprobado experimentalmente que esta reacción tiene una cinética de primer orden respecto de la sacarosa.
Definid el concepto de orden de reacción respecto de un reactivo. ¿Cuál de los siguientes gráficos (A, B o C) indica que la hidrólisis ácida de la sacarosa es de primer orden respecto de este reactivo? Razonad la respuesta.
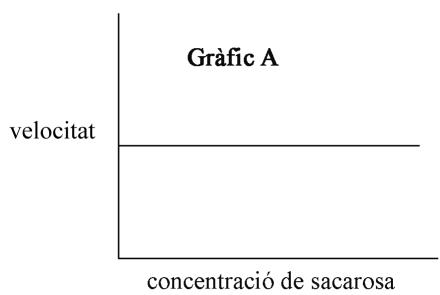
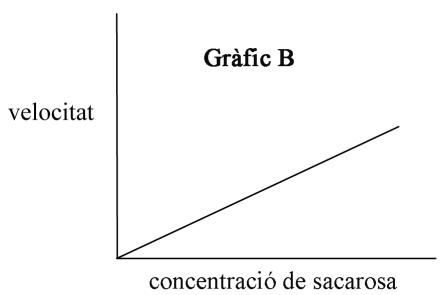
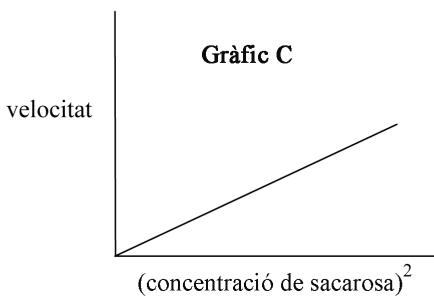
¿Qué es un catalizador? Explicad cómo actúa un catalizador en una reacción química a partir del modelo del estado de transición.
