Datos generales del examen
- Masas atómicas :
4Opción A
2 puntosBloque 4
Elegir una cuestión, 4A o 4B.
La Sierra Minera de Cartagena-La Unión ha sido explotada desde la Antigüedad, siendo fuente de riqueza y desarrollo, pero causando también un enorme impacto medioambiental, dramáticamente visible en la bahía de Portmán, que quedó enterrada bajo millones de toneladas de estériles mineros en la segunda mitad del S. XX. De las minas de la Unión se han extraído tres sulfuros: la galena (PbS), la blenda (ZnS) y la pirita .
La pirita no es un sulfuro de , sino un persulfuro de . Por su alto contenido en S se emplea, entre otros usos, para la obtención de ácido sulfúrico, siendo el primer paso la tostación de la pirita, proceso en el que se produce la oxidación tanto del Fe(II) como del S:
Indique cuál es el estado de oxidación del S en el .
Calcule la entalpía de reacción estándar de la tostación del , a partir de los siguientes datos:
La tostación de la pirita es un proceso exotérmico, pero aun así necesita altas temperaturas para vencer la energía de activación. Explique brevemente cuál de los siguientes diagramas entálpicos (perfiles de reacción) representa mejor el proceso (R y P indican reactivos y productos):
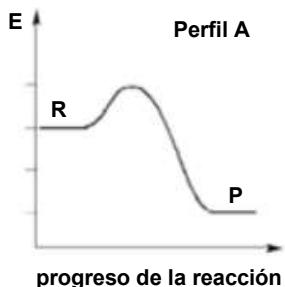
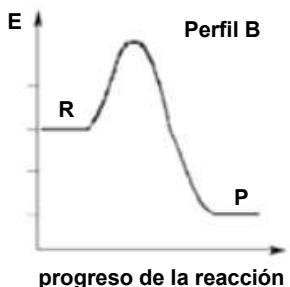
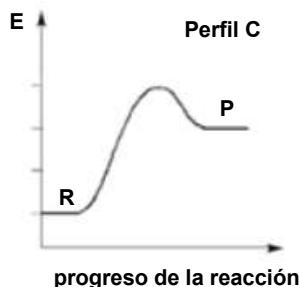
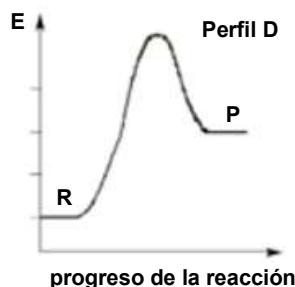
El obtenido a partir del se usa para la obtención de , según la siguiente reacción:
¿Cuántos moles de se obtendrán a partir de de pirita del de pureza en ?
