Los dos metales presentes en el ITO, el indio y el estaño, son elementos representativos y contiguos en el Sistema Periódico. Escriba sus símbolos atómicos e indique a qué periodo pertenecen.
QuímicaMurciaPAU 2025Ordinaria
Química · Murcia 2025
10 ejercicios90 min de duración
Datos generales del examen
- Masas atómicas :
Ejercicio 1 · Opción A
1Opción A
2 puntosBLOQUE 1
Elegir una cuestión, 1A o 1B.
El indio es un elemento metálico perteneciente al grupo de los boroideos o térreos y de alto valor económico por sus aplicaciones tecnológicas. Se utiliza para fabricar un compuesto denominado ITO (Indium Tin Oxide), un óxido de indio(III) dopado con óxido de estaño(IV), que es un componente de las pantallas táctiles.
Escriba las configuraciones electrónicas de ambos metales y, en base a ellas, justifique brevemente los estados de oxidación que presentan en el ITO, indicando qué electrones pierde cada uno de ellos.
El indio debe su nombre a una línea brillante de color índigo de su espectro atómico de emisión. Si un electrón excitado del indio se encuentra en un orbital 4f, indique qué valor tomará su número cuántico .
En la siguiente tabla se dan los valores de dos propiedades atómicas para el indio y el estaño. Explique brevemente cuál de ellos se corresponderá con el Elemento 1 y cuál con el Elemento 2.
| Elemento 1 | Elemento 2 | |
| Radio atómico (Å) | 1,56 | 1,45 |
| Energía de ionización (kJ·mol-1) | 558 | 709 |
Teniendo en cuenta la tabla anterior, explique brevemente a cuál de los dos elementos (1 o 2) corresponderá un valor de electronegatividad y a cuál un valor .
Ejercicio 1 · Opción B
1Opción B
2 puntosBLOQUE 1
Elegir una cuestión, 1A o 1B.
El (l) es un disolvente volátil, inflamable y tóxico, muy importante en muchos procesos industriales. Es un disolvente eficaz para aceites, ceras, azufre y muchos compuestos orgánicos. El (g) es un gas necesario para la vida en la Tierra, pero también es el causante del efecto invernadero.
Nombre ambas sustancias.
Represente sus estructuras de Lewis y explique brevemente cómo será su geometría y polaridad.
Justifique por qué el es un líquido a temperatura ambiente y el es un gas.
Explique si una disolución de azufre en conducirá la electricidad.
Ejercicio 2 · Opción A
2Opción A
2 puntosBLOQUE 2
Elegir una cuestión, 2A o 2B.
El es un antiácido que se toma para aliviar la acidez de estómago, causada principalmente por .
Escriba la reacción de neutralización que tiene lugar entre estos dos compuestos.
Teniendo en cuenta que el es inestable y descompone para dar y , calcule el volumen de (g), a y presión atmosférica, que se formará en la reacción de una pastilla que contiene de , con en exceso.
El anión es anfótero, lo que significa que puede actuar como un ácido () y como una base (). Escriba sus reacciones de hidrólisis ácida y básica y, sin necesidad de hacer cálculos, explique si, como resultado de ambas reacciones, una disolución de será neutra, ácida o básica.
Nombre los compuestos , y .
Ejercicio 2 · Opción B
2Opción B
2 puntosBLOQUE 2
Elegir una cuestión, 2A o 2B.
Las hormigas segregan como un mecanismo de defensa frente a otros insectos. Las abejas también lo producen, y lo utilizan para mantener limpia la colmena, ya que actúa como un desinfectante natural. Se trata de un ácido débil ().
Nombre el .
Si una hormiga roja emplea (nanogramos) de en cada mordisco, en un volumen de , ¿cuál es la concentración en del producido por la hormiga?
La disolución acuosa de segregada por las abejas melíferas produce, al disociarse, un pH de . Escriba la reacción de disociación del ácido y calcule su concentración inicial.
La del es diez veces menor que la del . Si se mide el pH en sendas disoluciones de los dos ácidos, de la misma concentración inicial, explique en cuál de ellas el pH será mayor.
Teniendo en cuenta la información del apartado d), calcule para el anión acetato.
Ejercicio 3 · Opción A
3Opción A
2 puntosBLOQUE 3
Elegir una cuestión, 3A o 3B.
Una de las mayores amenazas que se cierne sobre el Mar Menor es la eutrofización, proceso en el que un exceso de nutrientes produce un crecimiento desmesurado del fitoplancton (“sopa verde”), que impide que la luz solar llegue a las zonas más profundas, y que el resto de organismos fotosintéticos pueda seguir produciendo oxígeno (mueren las praderas de algas). Se genera así un desequilibrio entre los organismos consumidores de oxígeno, nutridos por el exceso de materia orgánica, y los que lo generan, causando episodios de hipoxia (muy bajos niveles de oxígeno) y la muerte masiva de la fauna del ecosistema.
Se considera que un ecosistema acuático está en peligro de hipoxia si la concentración de en el agua es inferior a . La determinación de este parámetro puede hacerse mediante el método de Winkler:
El primer paso consiste en fijar in situ el de la muestra de agua mediante la siguiente reacción redox:
Indique cuál es la especie oxidante y la reductora, y cómo varían sus números de oxidación.
Una vez en el laboratorio, el se reduce en medio ácido con , que se oxida a :
Ajuste esta reacción mediante el método del ion-electrón, escribiendo ambas semirreacciones.
Finalmente, el se valora con una disolución de tiosulfato sódico, que se oxida a tetrationato:
Indique el número de oxidación del S en las oxosales involucradas en esta reacción.
De todo lo anterior se deduce que el método Winkler sigue la siguiente secuencia estequiométrica:
1 mol moles ; 2 moles reaccionan con 4 moles de .
Si para una muestra inicial de de agua se consumieron en la valoración final moles de , calcule cuál era la concentración de en la muestra, en , y si hay riesgo de hipoxia.
Ejercicio 3 · Opción B
3Opción B
2 puntosBLOQUE 3
Elegir una cuestión, 3A o 3B.
La contaminación por nitratos se ha señalado como una de las causas de la eutrofización del Mar Menor y, a nivel mundial, afecta a la calidad de las aguas superficiales y subterráneas. Uno de los métodos propuestos para su eliminación es la desnitrificación electroquímica, en la que se consigue su transformación en los gases inocuos y . Aunque se trata de un proceso complejo, una versión global simplificada sería:
Indique qué compuesto se reduce, cómo varía su estado de oxidación y, por tanto, cuántos moles de electrones se intercambian tal y como está escrita la reacción (ya está ajustada).
Según la Ley de Faraday, , donde es la intensidad de corriente en amperios () y son los moles de electrones que circulan en la celda electrolítica. Calcule si para eliminar 40 moles de se han necesitado y explique si el resultado es coherente con el del apartado a).
Calcule qué volumen conjunto de y se habrá formado en el apartado b), a y .
Explique brevemente si durante el transcurso de la reacción el pH aumentará o disminuirá.
Indique cómo será el signo de y de para la reacción.
Ejercicio 4 · Opción A
4Opción A
2 puntosBLOQUE 4
Elegir una cuestión, 4A o 4B.
La Sierra Minera de Cartagena-La Unión ha sido explotada desde la Antigüedad, siendo fuente de riqueza y desarrollo, pero causando también un enorme impacto medioambiental, dramáticamente visible en la bahía de Portmán, que quedó enterrada bajo millones de toneladas de estériles mineros en la segunda mitad del S. XX. De las minas de la Unión se han extraído tres sulfuros: la galena (PbS), la blenda (ZnS) y la pirita .
La pirita no es un sulfuro de , sino un persulfuro de . Por su alto contenido en S se emplea, entre otros usos, para la obtención de ácido sulfúrico, siendo el primer paso la tostación de la pirita, proceso en el que se produce la oxidación tanto del Fe(II) como del S:
Indique cuál es el estado de oxidación del S en el .
Calcule la entalpía de reacción estándar de la tostación del , a partir de los siguientes datos:
La tostación de la pirita es un proceso exotérmico, pero aun así necesita altas temperaturas para vencer la energía de activación. Explique brevemente cuál de los siguientes diagramas entálpicos (perfiles de reacción) representa mejor el proceso (R y P indican reactivos y productos):
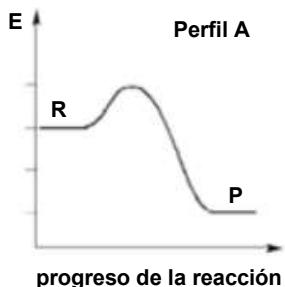
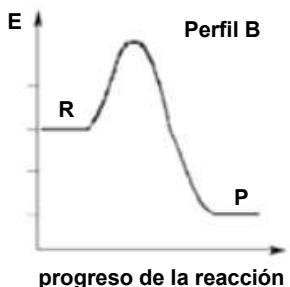
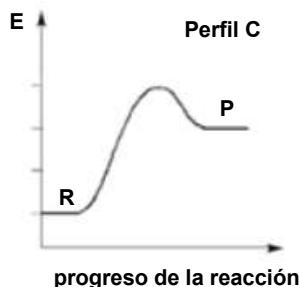
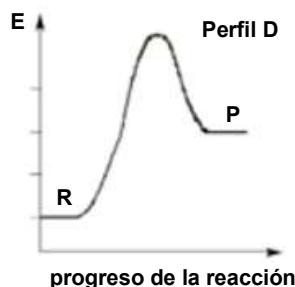
El obtenido a partir del se usa para la obtención de , según la siguiente reacción:
¿Cuántos moles de se obtendrán a partir de de pirita del de pureza en ?
Ejercicio 4 · Opción B
4Opción B
2 puntosBLOQUE 4
Elegir una cuestión, 4A o 4B.
La galena (PbS) era ya conocida y usada por los antiguos egipcios siendo, por ejemplo, el principal componente del kohl, un polvo cosmético usado como máscara de ojos. Sin embargo, el plomo es un elemento muy tóxico, que se acumula en el organismo y produce daños neurológicos (saturnismo).
Afortunadamente, la solubilidad del es muy pequeña (). Calcule las concentraciones de iones y en una disolución saturada de kohl (PbS).
Razone cualitativamente cómo variará la en un cierto volumen de disolución saturada de PbS si:
Se adiciona una sal soluble de , cuyo anión no interfiere con el equilibrio. Dato: el es aún más insoluble () que el PbS.
Se aumenta la T (la disolución de PbS en agua es un proceso endotérmico).
Se duplica la cantidad de .
En la galena argentífera, el PbS se encuentra asociado con . El Cabezo Rajao, en la Unión, debe su nombre a la explotación a cielo abierto de un filón de este mineral, en época romana. Si se procesaron un millón de toneladas de tierra con una riqueza media del en galena argentífera que, a su vez, contenía un en masa de , calcule la masa de Ag metálica que se obtuvo del yacimiento, suponiendo un aprovechamiento total en el proceso de extracción, separación y reducción de la Ag. Exprese el resultado con dos cifras significativas.
Ejercicio 5 · Opción A
5Opción A
2 puntosBLOQUE 5
Elegir una cuestión, 5A o 5B.
Dada la siguiente reacción:
Indique qué tipo de reacción es, y nombre el compuesto de Cr que actúa como catalizador.
Nombre el reactivo y el producto de la reacción, y explique brevemente si alguno de ellos puede presentar isomería espacial (óptica o geométrica).
Nombre los siguientes compuestos y explique brevemente si son isómeros (y de qué tipo), de algunas de las sustancias que participan en la reacción:
Uno de los cuatro compuestos orgánicos que aparecen en esta pregunta está siendo investigado como combustible alternativo, ya que puede obtenerse a partir de biomasa renovable. Cada mol produce, al quemarse, 2 moles de y 3 moles de . Indique qué compuesto es y escriba su reacción de combustión ajustada.
Ejercicio 5 · Opción B
5Opción B
2 puntosBLOQUE 5
Elegir una cuestión, 5A o 5B.
Los isómeros son compuestos que presentan la misma (1) pero cuyos átomos están enlazados de forma diferente (isomería (2)) o presentan una distinta disposición espacial (isomería (3)).
Un tipo de isómeros especialmente interesante son los enantiómeros, que son imágenes especulares no superponibles. Son tan similares entre sí que tienen idénticas propiedades físicas y químicas, excepto si éstas están relacionadas con factores de simetría espacial (como, por ejemplo, su interacción con la luz polarizada).
Complete los huecos del texto anterior con una o dos palabras, indicando en el cuadernillo de respuestas la numeración del hueco y la palabra (o palabras) que irían en él. No copie el texto completo.
Considere los siguientes pares de compuestos y copie y complete en el cuadernillo de respuestas la siguiente tabla, indicando la fórmula molecular de cada par de compuestos, si son, o no, isómeros estructurales o espaciales, y si la pareja tiene, o no, idéntico punto de fusión. (No se preocupe por la calidad del aspecto de la tabla en el cuadernillo de respuestas, sino por su claridad)
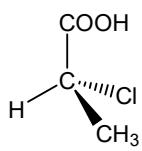
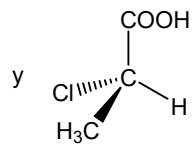
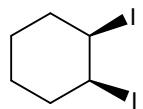
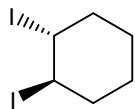
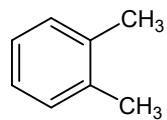
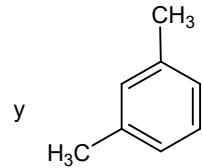
| Fórmulamolecular | ¿Isómerosestructurales? (Sí/No) | ¿Isómerosespaciales?(Sí / No) | ¿Idéntico puntode fusión? | |
| Pareja A | ||||
| Pareja B | ||||
| Pareja C |
Nombre los compuestos anteriores distinguiéndolos según su isomería (excepto en el caso de los isómeros ópticos, para los que no hace falta distinguirlos).
Elija una de las parejas anteriores y especifique para ella el tipo y subtipo de isomería.
El ácido ftálico es un importante compuesto químico que se utiliza para la fabricación de polímeros y resinas. Dibuje su fórmula e indique a partir de qué compuesto del apartado b) podrá obtenerse ácido ftálico mediante una reacción de oxidación (no es necesario que escriba dicha reacción).
