5Opción B
2 puntosLa molécula de -D-glucopiranosa se transforma en su isómero -D-glucopiranosa, en disolución acuosa y a . Este proceso se conoce con el nombre de mutarrotación.
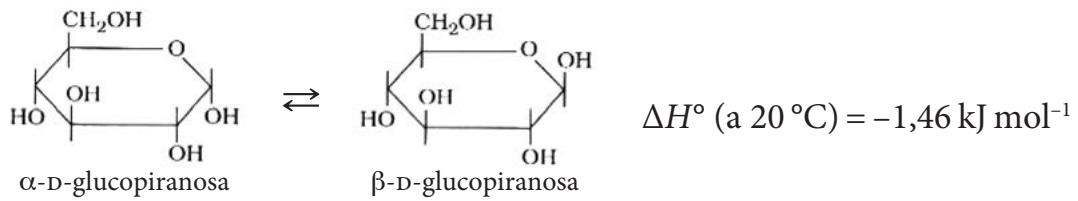
Una solución contiene en equilibrio un en masa de -D-glucopiranosa y un en masa de -D-glucopiranosa, a . ¿Qué valor tiene la constante de equilibrio en concentraciones, , de la reacción de mutarrotación de la -D-glucopiranosa a ?
La mutarrotación de la -D-glucopiranosa a sigue una cinética de primer orden con una constante de velocidad de . Dibujad, de manera aproximada, el perfil de esta reacción en un diagrama de la energía en función de la coordenada de la reacción, suponiendo que la reacción se lleva a cabo en una única etapa, e indicad dónde se encuentra la magnitud de la energía de activación. Cuando la reacción se produce en un medio fuertemente ácido, , la constante de velocidad tiene un valor de . Explicad razonadamente a qué se debe este cambio.
